Författare:
Kai Knudsen
Uppdaterad:
25 augusti, 2025
Här beskrivs principerna för respiratorbehandling vid akut lungsvikt samt vid uttalad lungsvikt med ARDS. Här beskrivs olika ventilatorinställningar och hur man behandlar svår andningssvikt. Här beskrivs också principerna vid behandling av svår Covid-19 infektion. Olika ventilatorinställningar (andningsmetoder - modus) i olika typer av ventilatorer presenteras liksom CPAP, BiPAP och Högflödesgrimma (Optiflow). Urträning ur respirator och lungrekrytering beskrivs här.
- Respiratorbehandling
- Ventilatorbehandling vid svår andningssvikt
- Respiratorbehandling vid ARDS
- ARDS vid Covid-19-infektion
- Finjusteringar i respiratorn
- Urträning ur respiratorn – ”weaning”
- Urträning ur respirator – praktiska råd
- Lungrekrytering
- Extubation
- Hosta – vid respiratorbehandling
- HFNC – högflödesgrimma – Optiflow
- CPAP – Continuous Positive Airway Pressure
- PEEP – Positive End-Expiratory Pressure
- ASV – Adaptive Support Ventilation
- BiPAP – Biphasic Positive Airway Pressure
- BiPAP-assist (med ASB)
- (S)CMV+
- APRV – Airway Pressure Release Ventilation
- DuoPAP andningsmönster
- IPPV – Intermittent Positive Pressure Ventilation
- MMV – Mandatory Minute Ventilation
- PCV+
- SIMV – Synchronized Intermittent Mandatory Ventilation
- SIMV ASB (Assisted Spontaneous Breathing)
- PSIMV+
- VK – Volymkontrollerad ventilation
- TK – Tryckkontrollerad ventilation
- TU – Tryckunderstödd ventilation
- VU – Volymsunderstödd ventilation
- VKTS – Volymkontrollerad tryckstyrning
- Automode VKTS – VU
- Automode VK – VU
- Automode TK + TU
- NAVA – Neurally Adjusted Ventilatory Assist
- Respiratorbehandling av barn
- Maquet/Siemens (Getinge) ventilatorer
- Aisys (ADU)(Datex-Ohmeda – GE Healthcare)
- Evita XL, Evita 4, Pulmovista (Drägers ventilatorer)
Respiratorbehandling
Patienter, som på grund av lungsjukdom eller annan skada på lungorna inte kan andas tillfredsställande, kan behandlas med hjälp av en respirator som ventilerar lungorna. Respiratorn beskrivs ofta som en ventilator. Andningen sker invasivt via ett slutet slangsystem med ett reglerat och kontrollerat tryck och flöde i luftvägarna. Ventilatorn levererar en förinställd tidalvolym eller minutvolym under en förinställd inspirationstid och vid en förinställd andningsfrekvens. Patienten är i regel oralt intuberad men kan även vara nasalt intuberad eller ansluten via en trakealkanyl i ett tracheostoma.
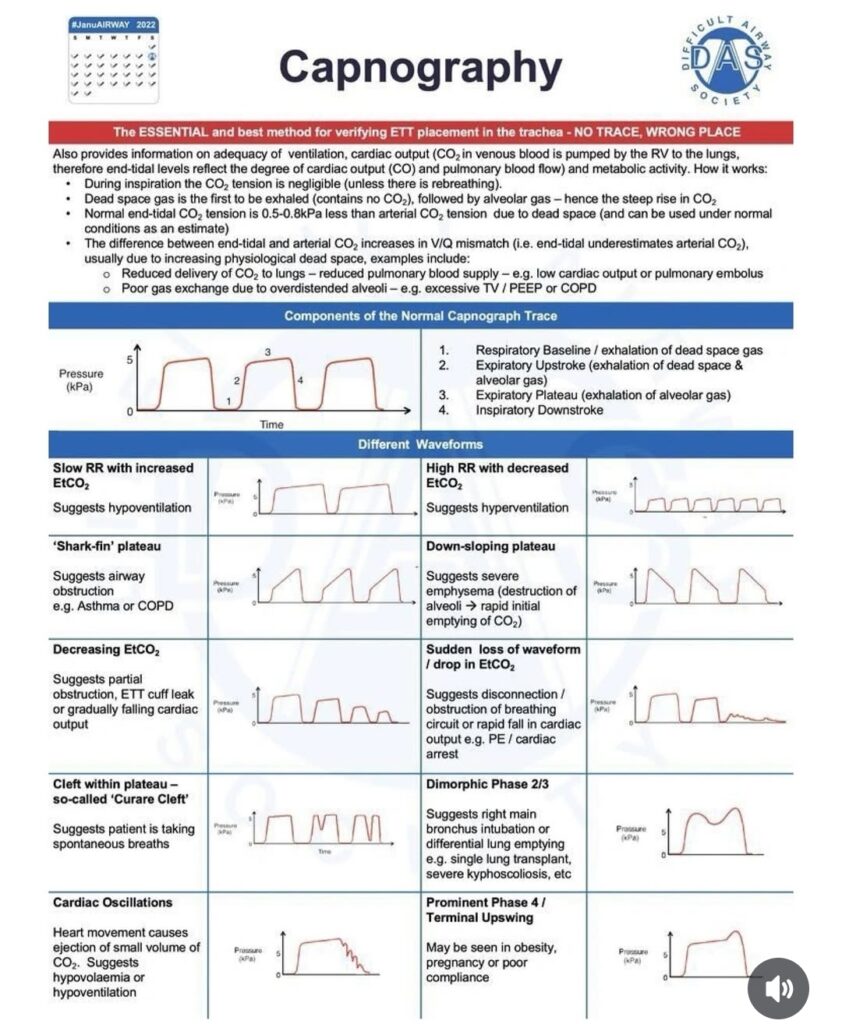
Normal spontanandning sker fysiologiskt med hjälp av undertryck i luftvägarna, luften sugs in i lungorna av andningsmuskulaturen medan i respiratorgenererad ventilation blåses luft in i lungorna under övertryck. Ventilatorns tryckluft genereras mekaniskt av en kompressor som normalt finns på baksidan av andningssystemet. Ett system av precisionsventiler kontrollerar sedan gastrycket och gasflödet till patienten som regleras av användaren digitalt eller analogt i olika andningsmetoder. Varierande andningsmetoder beskrivs ofta som ”ventilatorns mode” eller ”andningsmode” i respiratorn. En vanligare benämning är ”ventilatorinställningar” eller ”andningsmetod i respiratorn”.

De vanligaste grundinställningarna i respiratorns andningsmönster är antingen volymkontrollerad ventilation (VK 20-1500 ml/andetag, vanligen 450-550 ml) eller tryckkontrollerad ventilation (TK 5-60 cm H2O i inandningstryck, vanligen 10-12 cm H2O). De olika ventilatortinställningarna beskrivs i detalj nedan.
Exempel på olika ventilatortinställningar är:
- Volymkontrollerad tryckstyrning (VKTS)
- Tryckkontroll (TK)
- Volymkontroll (VK)
- ASV – Adaptive Support Ventilation
- APRV
- Duo PAP andningsmönster
- Bi-vent/APRV
- SIMV (TK) + TU
- SIMV (VKTS) + TU
- Automode TK + TU
- Automode VKTS – VU
- Tryckunderstöd (TU/CPAP) (PS/CPAP)
- Volymunderstöd (VU)
- Neuralt reglerat ventilationsstöd (NAVA)
Respiratorbehandling avlastar andningsarbetet men kan tyvärr tillfoga redan sjuka eller skadade lungor ytterligare skador pga. tryckskador, atelektaser, pneumothorax eller infektioner.
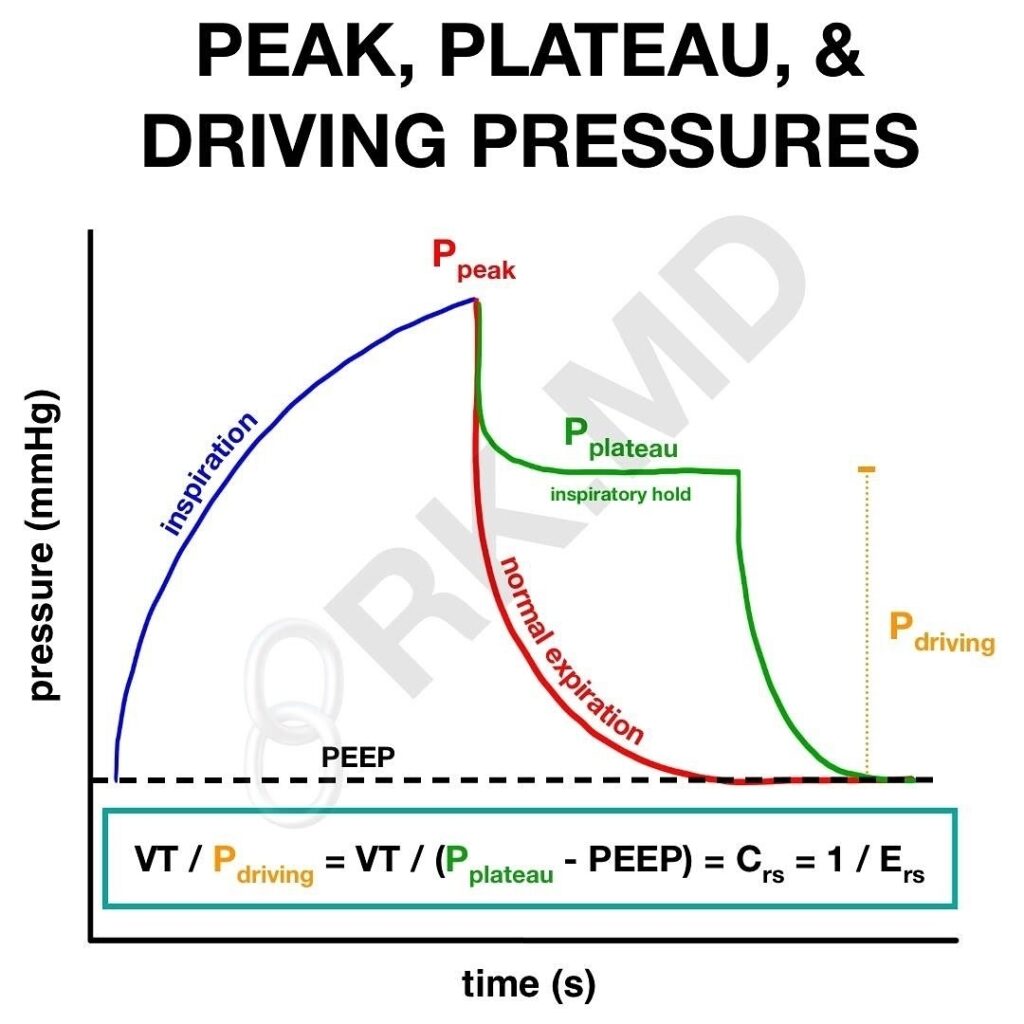
För att minimera risken för skador till följd av respiratorbehandling är det därför önskvärt att kunna anpassa behandlingen för varje enskild patient och belasta lungvävnaden så lite som möjligt. Kontrollerad ventilation innebär stora förändringar i lungvolymsförändringar och tryck i luftvägarna. Gasutbytet i lungorna påverkas av både ventilationen och cirkulationen. Vanliga orsaker till andningssvikt är lungödem, pneumoni, sepsis, atelektaser, svår KOL eller astma. Andra orsaker kan vara stort trauma, lungkontusioner, skalltrauma, stroke, läkemedelsöverdosering, förgiftningar, oklar medvetslöshet eller medtagen och utmattad patient. Kontrollerad ventilation sker vanligen med hjälp av en respirator. Antingen är patienten intuberad endotrakealt (invasiv ventilation) eller så sker ventilationen med hjälp av tättslutande mask, non-invasiv ventilation (NIV). Tub eller andningsmask kopplas till respiratorns slangsystem och dess andningsgaser.

Ventilatorbehandlingen är vanligen volymkontrollerad (VK/VCV) eller tryckkontrollerad (TK/PCV). Volymkontrollerad ventilation innebär att given volym i varje andetag är förutbestämd och tryckkontrollerad ventilation innebär att givet tryck i varje andetag är förutbestämt. Volymkontrollerad ventilation ger alltid ett konstant flöde i inandningsluften medan i tryckkontrollerad ventilation får man ett decelererande flöde.
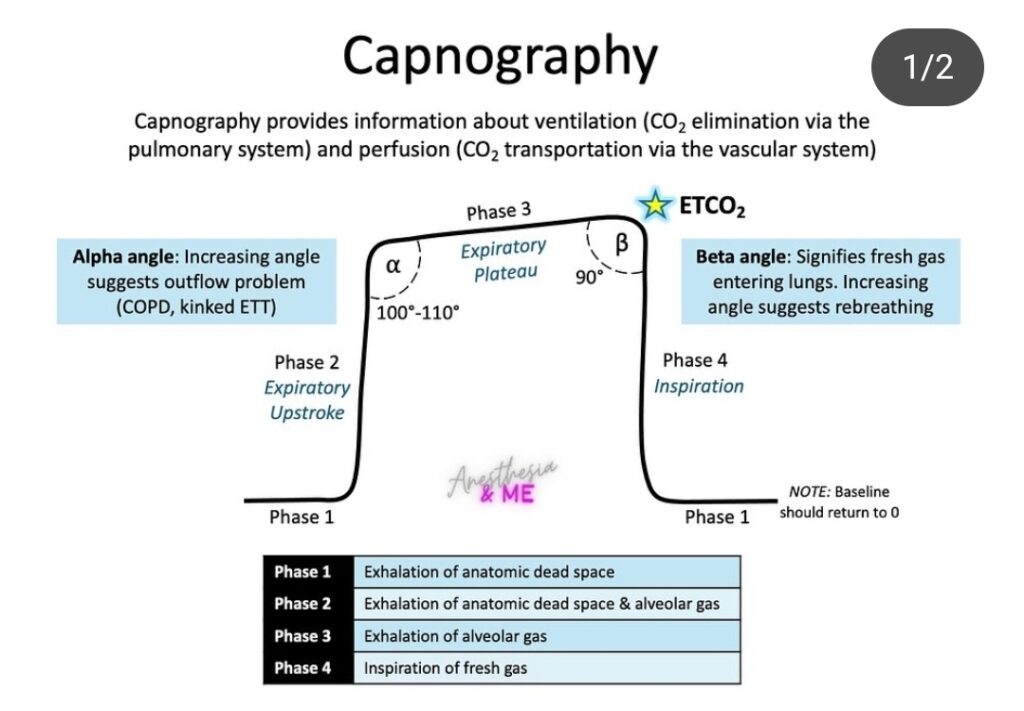

Tryckkontrollerad ventilation gynnar gasdistributionen och ger lägre topptryck jämfört med volymkontrollerad ventilation. Volymkontrollerad ventilation ger mindre risk för hypoventilation och kan vara av godo vid ARDS. Tiden patienten behandlas i respirator försöker man alltid minimera.
Ventilatorinställningar vid olika grader av lungsvikt
| Andningsfysiologiska parametrar | Frisk lunga | Måttlig lungsvikt | Svår lungsvikt |
|---|---|---|---|
| Andningsmode | TU, VK, VKTS, BiPAP | TU, VK, TK, VKTS, BiPAP | TK, (TU, VKTS), BiPAP |
| Tidalvolym ml/kg | <6-8 | <6-8 | <6-8 |
| Andningsfrekvens | 15-20 | 15-20 | 15-30 |
| I:E kvot | 1:2 | 1:2-1:1 | 1:1(-2:1) |
| PEEP cm H20 | 0-5 | 5-10 | 10-20 |
| Syrgashalt % | <40 | 40-60 | 40-100 |
| Lungrekrytering | - | Ja | Ja i tidigt skede |
Ventilatorbehandling vid svår andningssvikt
Patienter som vårdas utanför IVA
- O2-tillförsel med mål SpO2 92-96%; hos patienter med KOL eller risk för CO2-retention mål SpO2 88-92%1.
- När O2-tillförsel, inklusive tillförsel med reservoarmask, inte är tillräcklig, rekommenderas högflöde via näsgrimma (HFNC, ”Optiflow”).
- När HFNC inte är tillräckligt kan CPAP med tryck ≤ 10 cm H2O prövas.
- Erfarenheten är att COVID-19 patienter som är helt beroende av NIV, dvs. inte kan upprätthålla tillräckligt gasutbyte utan NIV, ofta fortsätter att försämras. Detta kan leda till behov av urakut intubation vilket innebär ökade risker för patienten ökad risk för smittspridning. För patienter med mindre uttalad lungsvikt kan NIV vara ett alternativ som används under längre tid, ev. alternerande med HFNC. På samma sätt kan NIV användas för patienter där intensivvård inte är aktuell men undviks om man skiftat till palliativ vård.
- HFNC, CPAP och NIV medför risk för aerosolbildning och smittspridning vilket stärker indikationen för skyddsutrustning. Jämfört med CPAP/NIV kan HFNC medföra en fördel genom mindre behov av att vara mycket nära patienten.
- HFNC och NIV ska inte användas vid transporter inom sjukhuset, reservoarmask används istället.
- Mobilisering, hosthjälp och lägesändringar är viktiga för att förebygga och behandla försämrad lungfunktion. Det har visat sig särskilt effektivt med framstupa sidoläge eller bukläge, med eller utan annat andningsstöd som HFNC, NIV eller CPAP.

Potentiella indikationer för respiratorvård
- PaO2/FIO2 < 20 kPa eller försämring med behov av ökande FIO2 (O2%), SpO2 <93% med O2 ≥ 10 L/min på mask.
- Stigande PCO2 (> 6.0 kPa), särskilt om pH < 7.30.
- Ökat andningsarbete och/eller andningsfrekvens (AF) > 30/min. Fråga patienten om det blivit bättre eller sämre med andningen över tid.
- När NIV används för patienter pga. att syrgas på reservoarmask eller HFNC är otillräcklig behandling och patienten fortsatt försämras eller att patienten inte har förbättrats inom 1-2 h efter behandlingsstart.
- Påverkad medvetandegrad.
- Hypotension, oliguri, förhöjt och stigande P-Laktat, hjärteko med uttalad höger och/eller vänstersvikt.
- Innan IVA-kontakt tas, ska, i normalfallet, ev. behandlingsbegränsningar ha diskuterats på vårdande enhet redan innan patienten läggs i respirator. Om patienten uppfyller någon IVA-indikation ska IVA-kontakt tas parallellt med att denna diskussion genomförs. Ansvaret för detta ligger primärt hos ansvarig läkare på den avdelning där patienten vårdas.
Intubation
Intubationsproceduren är kopplad till en ökad risk för risk för cirkulatorisk/respiratorisk kollaps och för smitta av personalen, särskilt för den som intuberar. COVID-19 patienter kan se relativt opåverkade ut trots signifikant hypoxi och hög andningsfrekvens. De kan försämras mycket snabbt och har sedan mycket svårt att återhämta sig efter intubation. Det är därför en stark rekommendation att inte vänta för länge med intubation. Intubation av COVID-19 patienter innebär alltid en ökad risk för smittspridning. För procedur och checklista se särskild riktlinje, https://sfai.se/download-attachment/11747.
Rekommendationer avseende ventilatorbehandling
Befuktning/filter
Sekretstagnation och ”tubstopp” är relativt vanligt, aktiv befuktning med konventionell utrustning är förshandsval. Om aktiv befuktning inte används ges passiv befuktning med HME med filterfunktion. Använd alltid filter vid ventilatorns expirationsingång. Alla byten av filter/slangar görs med ventilatorn i standby. Auto-PEEP och patient-ventilator dyssynkroni kan bero på filter som behöver bytas – särskilt om patienten har aktiv befuktning och/eller inhalationer. Test av nya slangar kan hoppas över i samråd med ansvarig läkare.
Sugsystem
Slutet system används alltid vid Covid 19 infektion.
Tidalvolym/Drivtryck
Generellt accepteras tidalvolym upp till 8 ml/kg PBW om drivtryck ≤ 15 cm H2O och platåtryck ≤ 30 cm H2O. Större tidalvolym/drivtryck accepteras när reduktion är omöjlig eller kräver åtgärder som bedöms försämra situationen som ökad sedering, behov av relaxation eller försämrat gasutbyte.
PEEP
Väljs individuellt, om bra compliance ofta 6-12 cm H2O även vid högre FIO2. Pröva högre PEEP om lägre compliance och lågt PaO2/FIO2. Omvärdera högt PEEP genom reduktion med 2 cmH2O och uppföljning av tidalvolym, compliance och gasutbyte. Observera att compliance bara kan värderas vid kontrollerad ventilation.
SpO2/PaO2 – målvärden:
- 88-94%, 7,5-9,5 kPa om kontrollerad ventilation
- 92-94% 8,5-9,5 kPa om understödd ventilation
PaCO2
Upp till 8.0 kPa accepteras generellt. Högre PaCO2 kan accepteras om pH > 7,20 med samtidig rimlig andningsdrive. Högre PaCO2 kan också accepteras om ventilationen annars medför alltför höga tidalvolymer/drivtryck eller signifikant auto-PEEP.
Lungrekrytering
Övervägs tidigt om lågt PaO2/FIO2 och låg compliance, särskilt om plötslig försämring. Uteslut bronkintubation, sekret/hotande tubstopp, pneumothorax. Upprepa inte rekrytering om föregående rekrytering inte haft effekt.
Patient-ventilator dyssynkroni
Hanteras primärt med justering av ventilatorinställningar och ökad sedering, i andra hand med muskelrelaxantia intermittent eller infusion som ska omprövas efter 12- 24 h.
Buklägesbehandling
Rekommenderas om PaO2/FIO2 < 20 kPa och även vid PCO2-problem, sträva efter minst 16 h/dygn, daglig vändning med 4-6 h i ryggläge.
Urträning
Pga. långsam förbättring och risk för ”bakslag” påbörjas regelrätt urträning relativt sent i förloppet och först vid lägre ventilatorinställningar än vad som annars är vanligt.
Befuktning/användning av filter i ventilatorkretsen (”slangarna”) vid misstänkt eller säkerställd COVID-19
Balansera mellan risk för smittspridning och vad som är optimalt för patienten.
- Gör ett patient- och situationsbaserat val mellan aktiv och passiv befuktning. Aktiv befuktning är att föredra. Indikation för aktiv befuktning föreligger särskilt vid uttalad hyperkapné med behov av att eliminera dead space eller vid segt/torrt sekret. Torrt/segt sekret kan orsaka tubstopp eller auto-PEEP. Om aktiv befuktning inte är möjlig kan man överväga t.ex. acetylcysteininhalationer men då via ett ”slutet” nebuliseringssystem.
- Passiv befuktning görs i första hand med HME (fukt-värme-växlare) som också har filterfunktion. Denna ska placeras så nära tuben som möjligt men det slutna sugsystemet måste vara mellan tuben och HME/filtret.
- Om HME med filterfunktion saknas används annan HME som kompletteras med filter vid ventilatorns inspirationsutgång.
- Det ska alltid finnas ett filter på exspirationsingången på ventilatorn.
- Om aktiv befuktning används ska HME/filter vid tuben inte användas, däremot ska det finnas ett filter vid ventilatorns inspirationsutgång.
- Vid alla filterbyten, slangbyten och liknande ska tuben kortvarigt klampas och ventilatorn sättas i Stand-By innan isärkopplingar görs. Ventilatorn startas inte förrän man säkerställt att allt kopplats ihop igen. För trakeotomerade patienter görs detta på samma sätt men utan klampning.
Invasiv ventilation
- Med tryckkontroll väljs drivtryck för önskad tidalvolym, sedan justeras AF till önskad minutventilation och ett acceptabelt PaCO2 men undvik auto-PEEP.
- Acceptera tidalvolym ca. 8 ml/kg PBW (predicted body weight) om drivtrycket ≤15 cm H2O (drivtryck = tryck över PEEP, det ventilerande trycket). Sträva succesivt mot lägre tidalvolym /kg PBW om drivtrycket är högre.
- Observera att drivtrycket egentligen bara kan bedömas vid kontrollerad ventilation. Vid tryckunderstödd ventilation är förslaget att acceptera tidalvolymer upp till 8 ml/kg PBW förutsatt att understödet är max 14 cm H2O och patientens inte själv ”drar” mycket på inandningen. Kan detta inte uppnås föreslås kontrollerad ventilation eller åtgärder för att minska andningsdriven t.ex. ökad sedering.
- Observera att reduktion av tryckunderstöd för att minska tidalvolymen ofta ger liten effekt men leder till ökat andningsarbete. Det är därför sällan lämpligt med tryckunderstöd < 8-10 cm H2O. Vid höga tidalvolymer kan det vara korrekt att öka tryckunderstödet om patienten har ett stort andningsarbete. Resultatet blir ofta oförändrad tidalvolym men med minskat andningsarbete. Alternativet är att byta till kontrollerad ventilation.
- Större tidalvolym/drivtryck accepteras när reduktion är omöjlig eller där alternativet är åtgärder som bedöms försämra situationen, tex djupare sedering, behov av muskelrelaxation, försämrat gasutbyte, uttalad patient-ventilatordyssynkroni.
- Målet är topptryck ≤ 30 cm H2O och drivtryck ≤ 15 cm H2O. Sträva alltid efter lägsta möjliga drivtryck.
- FiO2 med mål SpO2 88-94%, och 92-94% om tryckunderstödd ventilation.
- PEEP väljs individuellt, ofta 6-12 cm H2O. Ofta väljs lägre PEEP än vid annan ARDS, särskilt om patienten har hög compliance (> compliance 30 ml/cm H2O).
- Vid behov av högt FIO2, dvs. måttlig-svår ARDS kan högre PEEP prövas, särskilt vid låg compliance. Om högre PEEP inte ger förbättrat gasutbyte eller förbättrad compliance, eller om ökad PEEP leder till hemodynamisk försämring, återgår man till lägre PEEP. På samma sätt bör PEEP >8-10 cm H2O omprövas minst dagligen men efterfråga först effekten av tidigare försök till reduktion. Förändringar görs i steg om 2 cm H2O.
- Hyperkapné pga. försvårad CO2-elimination accentueras av högt PEEP, särskilt vid relativ hypovolemi. Överväg att ge volym och att reducera PEEP, ett lägre PEEP kan totalt sett vara bättre även om det medför att FIO2 måste ökas.
- Överväg tidig lungrekrytering med ökat PEEP och ökade luftvägstryck om patienten har lågt PaO2/FIO2 och låg compliance (< c. 20 ml/cm H2O) men rekrytera med ökad försiktighet vid hypovolemi/hemodynamisk instabilitet. Upprepa inte rekryteringsförsök om de tidigare inte gett effekt.
- Patient-Ventilator dyssynkroni. När patienten är svårventilerad och inte följer ventilatorn (”andas emot”) hanteras det med ökad sedering (inkl. ökad opiatdos). Om inte detta är tillräckligt kan upprepade doser muskelrelaxation eller infusion i upp till 24-48 h prövas. Vid mycket svår gasutbytesstörning rekommenderas försiktighet vid skifte från understödd till kontrollerad ventilation. Risken är att detta skifte kan orsaka respiratorisk kollaps. Lösningen kan då vara snabb återgång till spontanandning med understödd ventilation t.ex. med reversering av läkemedel.
Undvik aerosolbildning genom att så långt som möjligt inte koppla isär ventilatorslangarna/tuben. Den här rekommendationen syftar också till att undvika derekrytering (atelektasbildning).
- Använd slutet sugsystem.
- Undvik inhalationsbehandling förutom vid stark indikation.
- Minimera antalet bronkoskopier. Bronkoskopi görs för diagnostik och vid överhängande risk för tubstopp. Använd muskelrelaxantia vid bronkoskopi, men med beredskap för reversering (se kommentar i stycket om patient-ventilator dyssynkroni ovan). Blind skyddad borste är ett alternativ för diagnostik.
- Om isärkoppling är oundviklig skall ventilatorn sättas i Stand-By och tuben klampas med peang. Överväg sederingsbolus innan detta görs. Skifta till aktiv ventilation först när alla slangar är ihopkopplade.
Buklägesbehandling minst 16 h/dag rekommenderas om PaO2/FIO2 < 20 kPa i ryggläge. Bukläge vid COVID-19 ARDS har ofta en gynnsam effekt och kan därför prövas vid högre PaO2/FIO2, t.ex. vid successiv försämring av syresättningen eller när problemet mer är hyperkapné än hypoxemi. Om ”äkta bukläge” är svårt att åstadkomma är framstupa sidoläge ett alternativ. I båda fallen bör små justeringar göras så att tryckpunkter och huvudets/nackens position växlar regelbundet.
Andra ventilationssätt: Det finns inga studier som visat tydliga fördelar med att använda andra ventilationssätt än tryckkontroll och tryckunderstöd. I nuvarande situation med mycket skiftande erfarenhet och kompetens hos både läkare och omvårdnadspersonal rekommenderas att man avstår från att använda ventilationssätt som inte används i vanliga fall. Dvs. använd enbart tryckkontroll och tryckunderstöd. Tryckstyrd ventilation med kontrollerade tidalvolymer t.ex. VKTS används i särskilda fall där stabila PaCO2-nivåer krävs.
Sedering/Urträning
Om patienten har välfungerande kontrollerad ventilation så ska man inte ha bråttom med att skifta till tryckunderstöd. Vänta till PaO2/FIO2 ≥ 33 kPa (motsvarar ungefär SpO2 95% vid FIO2 0.3) och att patienten vid understödd ventilation inte andas med alltför stora tidalvolymer (t.ex. > 10 ml/kg PBW). Av samma skäl bör PEEP inte reduceras till <6 cm H2O förrän i ett relativt sent skede i förloppet. Uttalat försämrad syresättning vid vändningar indikerar att patienten inte är redo för extubation. Erfarenhet hittills är att patienter med COVID-19 ARDS kräver minst 10-14 dagars intensivvård. Under pågående intensivvård skall patienten betraktas som smittsam. Extubation bör göras i ett senare skede av förloppet, dvs. i en situation där behovet av fortsatt andningsstöd efter extubationen bedöms som lågt.
Extubation
Flera centra har rapporterat luftvägshinder efter extubation, det är oklart om och varför detta kan vara vanligare vid COVID-19 än annan pneumoni/ARDS. Sekretstagnationsproblem är vanligt efter extubation, det hanteras på vanligt sätt med hosthjälp och mobilisering. Sannolikt kan trackeotomi i utvalda fall medge mindre risk för reintubation och ett snabbare avslut av intensivvården men det förutsätter att patienten kan skrivas ut till vårdenheter med rätt kompetens och bemanning.
Refraktär hypoxemi/hyperkapné
Möjliga åtgärder är rekrytering, bukläge, optimera PEEP (kan betyda sänkning av PEEP), minimera apparat dead space, hemodynamisk bedömning/optimering (uteslut hypovolemi som orsak till försämrad CO2-elimination), fördjupad sedering, neuromuskulär blockad, behandla feber, acceptans av spontanandning/understödd ventilation trots större tidalvolymer/luftvägstryck än önskat, inhalation av vasodilaterande läkemedel (finns positiva erfarenheter från inhalation av iloprost och milrinon), samråd med ECMO. En hög frekvens av lungembolism hos COVID-19 patienter beskrivits vilket stärker indikationen för diagnostik avseende detta.
ECMO
Överväg kontakt med ECMO om patienten inte förbättras med de tidigare nämnda åtgärder och svår hypoxemi kvarstår (t.ex. PaO2/FiO2 <10 KPa) och inga kontraindikationer föreligger. Indikationen för ECMO kan komma att förändras under epidemin.
Trackeotomi
Använd skyddsutrustning, använd muskelrelaxantia för att undvika hosta, täck gärna ansiktet/tuben med plastduk, ställ ventilatorn i stand-by när tuben backas och trakea ska incideras. Säkerställ att alla slangar är kopplade och att kanylen är kuffad innan ventilatorn startas igen. Se länk för beskrivning av ARDS vid COVID 19 och referenser
Respiratorbehandling grafik
Klicka på bilden för att hämta PDF-filen

Respiratorbehandling vid ARDS
Definition av ARDS
- Akut lungsvikt (≤ 7 dagar)
- Lungsvikten förklaras inte helt av hjärtsvikt
- Bilaterala infiltrat (röntgen/CT/ultraljud)
- PaO2/FiO2 < 40 kPa trots PEEP 5 cm H2O
Gradering av ARDS
| ARDS | PFI (kPa) = PaO2/FiO2 | FiO2 för PaO2 10 (SpO2 ≈ 95 %) | FiO2 för PaO2 8 (SpO2 ≈ 90 %) |
|---|---|---|---|
| Mild | 40.0-26.6 | 25% | 21% |
| Måttlig | 26.6-13.3 | 37% | 30% |
| Svår | ≤ 13.3 | 75% | 60% |
Övergripande rekommendationer
- Undvik positiv vätskebalans om möjligt, allt viktigare med ökande grad av ARDS.
- Med ökande grad av ARDS uppkommer ett ökat behov av hemodynamisk utvärdering (hjärteko) och särskilda åtgärder om högersvikt förekommer.
- Säkerställ adekvat diagnostik och behandling av etiologin, infektionsdiagnostik och infektionsbehandling.
- Sederingsgrad väljs för patientkomfort, undvik för högt andningsarbete (om TU) och undvik patient – ventilator dyssynkroni.
- Profylax avseende DVT, stressulcus, VAP och trycksår
Beslutsstöd vid tidig ARDS
| Klassifikation | Åtgärder | Behandlingsmål |
|---|---|---|
| Lindrig ARDS PFI 26.7-40 kPa | Gynnsamt kroppsläge Om ej intuberad: Högflödesgrimma ≥40 L/min alt. NIV med PEEP ≥ 6, TU ≤ 5. Om intuberad: Ofta TU/CPAP: PEEP ≥ 8, TV ≤ 8 ml/kg Initiera adekvat antimikrobiell behandling Undvik positiv vätskebalans om möjligt | Mål: SpO2 : 92-95%, PaO2 : 9-10 AF < 7 Behandling syftar f.ö. till att • Minska kraftigt andningsarbete • Undvika stora tidalvolymer • Minimera patient/ventilator-dyssynkronier Om ej bättre i NIV ≤ 2 h ➔ ev intubation |
| Måttlig ARDS PFI 26.7-13.3 kPa | Ofta behov av intubation, särskilt om PFI <20: • Oftast PEEP 10-14 • Mål TV: ≤ 6 ml/kg PBW • Oftast kontrollerad ventilation • Ventilerande tryck: om TU: 8-14, om TK: ≤15 • Om kraftig andningsdrive/stora TV, öka sedering Vid PFI < 20: bukläge 16-20 h/dag (om ej kontraindicerat) | Mål: SpO2 90-94%, PaO2 8-10, Vid TK: pH >7.25 PaCO2 : ≤ 7(-8) Vid negativ PFI-trend trots adekvat behandling, betrakta och hantera som svår ARDS. Mål även som i åtgärdsrutan till vänster. |
| Svår ARDS PFI <13.3 kPa | Invasiv ventilation i kontrollerat mode (TK) TV ≤ 6 ml/kg PBW TK över PEEP: ≤ 15 Ptopp < 30, Oftast PEEP 12-18, titreras (Obs compliance och hemodynamik) AF bestämmer MV (mål pH >7,25, PCO2 <7-8) Om inte kontraindicerat: • Bukläge 16-20 t/dag • Sedering till komfort och utslagen egenandning • Neuromuskulär blockad om svår dysynkroni • Hjärteko för hemodynamisk bedömning • ECMO-kontakt vid fortsatt negativ trend (PFI<10) | Mål: SpO2 88-94 %, PaO2 7.5-10, pH >7.25 PaCO2 : ≤ 7-8 • Undvika eget andningsarbete • Om möjligt negativ vätskebalans • Försiktighet med rekrytering med ventilator men pröva vid plötslig försämring och som rescueåtgärd • Hemodynamisk optimering, högerkammaravlastning v.b. |
Vid ARDS ser man ofta, men inte alltid, en korrelation mellan grad av syresättningsproblem (lägre PaO2/FIO2) och lägre compliance. Detta beror på stora lungdelar som inte är gasfyllda/ventilerade. När en mindre del av lungorna ventileras blir compliance lågt och blodflödet genom oventilerade delar blir en intrapulmonell shunt, vilket i sin tur förklarar hypoxemi som svarar dåligt på ökat FIO2. Med den här patofysiologin ses ofta, men inte alltid, förbättrad syresättning och compliance med ökat PEEP och efter lungrekrytering med höga luftvägstryck. Mekanismen är då att lungdelar som tidigare inte var gasfyllda/ventilerade öppnas, vilket i sin tur betyder att större delar av lungan ventileras vilket ger bättre compliance och mindre shunt. Detta är logiken när behov av ökat FIO2 kopplas till användning av högre PEEP (PEEP-FIO2 tabeller). Under de senaste månaderna har det pågått en intensiv diskussion huruvida COVID-19 orsakad ARDS på ett systematiskt sätt skiljer sig från annan ARDS, t.ex. orsakad av pneumoni. I flera, relativt stora, patientmaterial har man dock haft svårt att påvisa kliniskt signifikanta skillnader för t.ex. compliance.
Samtidigt har vi också lokalt gjort erfarenheten att det är relativt vanligt med kombinationen svår ARDS (lågt PaO2/FIO2 kvot) och relativt hög (nästan normal) compliance, men detta förekommer också vid ARDS av annan etiologi än COVID-19. För alla patienter med ARDS, oavsett etiologi, behöver valet av behandling, t.ex. ventilatorinställningar, kontinuerligt anpassas efter den aktuella situationen. Ett exempel på detta är när stora syressättningsproblem (lågt PaO2/FIO2) är förenat med välbevarad, närmast normal, compliance. Bevarad compliance indikerar att lågt PaO2/FIO2 inte förklaras av lungdelar utan ventilation, vilket i sin tur betyder att det finns sämre förutsättningar för högre PEEP att förbättra gasutbyte eller compliance, Välbevarad compliance och frånvaron av större lungdelar som inte är gasfyllda/ventilerade är väl förenligt de röntgenfynd som är vanligast vid COVID-19 pneumoni: infiltrat av groundglass typ och frånvaron av större konsoliderade lungdelar.
Syresättningsproblemet i den här situationen har istället förslagits bero på V/Q mismatch i kombination med hämmad hypoxisk vasokonstriktion. Det är i den här situationen som något lägre PEEP och något högre tidalvolymer blir rimliga. Högt PEEP kan genom flera mekanismer försämra gasutbytet, särskilt CO2-eliminationen. Detta är inte specifikt för COVID-19 patienter men det blir särskilt viktigt eftersom det tycks vanligare att PEEP inte öppnar oventilerade lungdelar. Försämringen av gasutbytet vid ökat PEEP blir mer uttalad om patienten samtidigt är relativt hypovolem. Vid bevarad lungcompliance får PEEP större effekt på preload än vid ARDS med sänkt compliance. Försämrad cardiac output betingat av högt PEEP och relativ hypovolemi har föreslagits bidra till akut njursvikt hos COVID-19 patienter. Hos andra patienterna med COVID-19 pneumoni beskrivs en patofysiologi som är mer typisk för ”vanlig” ARDS: sänkt compliance och shunt pga. lungdelar som inte är gasfyllda/ventilerade kombinerat med förbättrat gasutbyte vid ökat PEEP/lungrekrytering. I den här situation stärks indikationen för att begränsa tidalvolymen och att pröva högre PEEP.
Diskussionen om ARDS av olika typ kommer sannolikt att fortgå. Oavsett detta så tycks den samlade erfarenheten tala för större restriktivitet med högre PEEP och acceptans för högre tidalvolymer än vid COVID-1 ARDS men också att det kan finnas patienter/situationer där patofysiologin mer liknar ”vanlig” ARDS.
ARDS vid Covid-19-infektion
Vid ARDS ser man ofta, men inte alltid, en korrelation mellan grad av syresättningsproblem (lägre PaO2/FIO2) och lägre compliance. Detta beror på stora lungdelar som inte är gasfyllda/ventilerade. När en mindre del av lungorna ventileras blir compliance lågt och blodflödet genom oventilerade delar blir en intrapulmonell shunt, vilket i sin tur förklarar hypoxemi som svarar dåligt på ökat FIO2. Med den här patofysiologin ses ofta, men inte alltid, förbättrad syresättning och compliance med ökat PEEP och efter lungrekrytering med höga luftvägstryck. Mekanismen är då att lungdelar som tidigare inte var gasfyllda/ventilerade öppnas, vilket i sin tur betyder att större delar av lungan ventileras vilket ger bättre compliance och mindre shunt. Detta är logiken när behov av ökat FIO2 kopplas till användning av högre PEEP (PEEP-FIO2 tabeller). Under de senaste månaderna har det pågått en intensiv diskussion huruvida COVID-19 orsakad ARDS på ett systematiskt sätt skiljer sig från ARDS, t.ex. orsakad av annan pneumoni. I flera, relativt stora, patientmaterial har man dock haft svårt att påvisa kliniskt signifikanta skillnader för t.ex. compliance.
Samtidigt har vi också lokalt gjort erfarenheten att det är relativt vanligt med kombinationen svår ARDS (lågt PaO2/FIO2 kvot) och relativt hög (nästan normal) compliance, men detta förekommer också vid ARDS av annan etiologi än COVID-19. För alla patienter med ARDS, oavsett etiologi, behöver valet av behandling, t.ex. ventilatorinställningar, kontinuerligt anpassas efter den aktuella situationen. Ett exempel på detta är när stora syressättningsproblem (lågt PaO2/FIO2) är förenat med välbevarad, närmast normal, compliance. Bevarad compliance indikerar att lågt PaO2/FIO2 inte förklaras av lungdelar utan ventilation, vilket i sin tur betyder att det finns sämre förutsättningar för högre PEEP att förbättra gasutbyte eller compliance, Välbevarad compliance och frånvaron av större lungdelar som inte är gasfyllda/ventilerade är väl förenligt de röntgenfynd som är vanligast vid COVID-19 pneumoni: infiltrat av groundglass typ och frånvaron av större konsoliderade lungdelar.
Syresättningsproblemet i den här situationen har istället förslagits bero på V/Q mismatch i kombination med hämmad hypoxisk vasokonstriktion. Det är i den här situationen som något lägre PEEP och något högre tidalvolymer blir rimliga. Högt PEEP kan genom flera mekanismer försämra gasutbytet, särskilt CO2-eliminationen. Detta är inte specifikt för COVID-19 patienter men det blir särskilt viktigt eftersom det tycks vanligare att PEEP inte öppnar oventilerade lungdelar. Försämringen av gasutbytet vid ökat PEEP blir mer uttalad om patienten samtidigt är relativt hypovolem. Vid bevarad lungcompliance får PEEP större effekt på preload än vid ARDS med sänkt compliance. Försämrad cardiac output betingat av högt PEEP och relativ hypovolemi har föreslagits bidra till akut njursvikt hos COVID-19 patienter. Hos andra patienterna med COVID-19 pneumoni beskrivs en patofysiologi som är mer typisk för ”vanlig” ARDS: sänkt compliance och shunt pga. lungdelar som inte är gasfyllda/ventilerade kombinerat med förbättrat gasutbyte vid ökat PEEP/lungrekrytering. I den här situation stärks indikationen för att begränsa tidalvolymen och att pröva högre PEEP.
Diskussionen om ARDS av olika typ kommer sannolikt att fortgå. Oavsett detta så tycks den samlade erfarenheten tala för större restriktivitet med högre PEEP och acceptans för högre tidalvolymer än vid COVID-1 ARDS men också att det kan finnas patienter/situationer där patofysiologin mer liknar ”vanlig” ARDS.
Litteratur
| Referenser andningssvikt Covid-19 Corona |
|---|
| O’Driscoll BR, Howard LS, Earis J, Mak V, British Thoracic Society Emergency Oxygen Guideline G, Group BTSEOGD. BTS guideline for oxygen use in adults in healthcare and emergency settings. Thorax. 2017;72(Suppl 1):ii1-ii90 |
| Tran K, Cimon K, Severn M, Pessoa-Silva CL, Conly J. Aerosol generating procedures and risk of transmission of acute respiratory infections to healthcare workers: a systematic review. PLoS One. 2012;7(4):e35797. |
| Peng PWH, Ho PL, Hota SS. Outbreak of a new coronavirus: what anaesthetists should know. Br J Anaesth. 2020;124(5):497-501. |
| Hui DS, Chow BK, Lo T, Tsang OTY, Ko FW, Ng SS, et al. Exhaled air dispersion during high-flow nasal cannula therapy versus CPAP via different masks. Eur Respir J. 2019;53(4). |
| Murthy S, Gomersall CD, Fowler RA. Care for Critically Ill Patients With COVID-19. JAMA. 2020;323(15):1499-500. |
| Maggiore SM, Lellouche F, Pigeot J, Taille S, Deye N, Durrmeyer X, et al. Prevention of endotracheal suctioninginduced alveolar derecruitment in acute lung injury. Am J Respir Crit Care Med. 2003;167(9):1215-24. |
| Papazian L, Aubron C, Brochard L, Chiche JD, Combes A, Dreyfuss D, et al. Formal guidelines: management of acute respiratory distress syndrome. Ann Intensive Care. 2019;9(1):69. |
| Amato MB, Meade MO, Slutsky AS, Brochard L, Costa EL, Schoenfeld DA, et al. Driving pressure and survival in the acute respiratory distress syndrome. N Eng J Med. 2015;372(8):747-55. |
| Fan E, Del Sorbo L, Goligher EC, Hodgson CL, Munshi L, Walkey AJ, et al. An Official American Thoracic Society/European Society of Intensive Care Medicine/Society of Critical Care Medicine |
| Clinical Practice Guideline: Mechanical Ventilation in Adult Patients with Acute Respiratory Distress Syndrome. Am J Respir Crit Care Med. 2017;195(9):1253-63. |
| Gattinoni L, Chiumello D, Caironi P, Busana M, Romitti F, Brazzi L, et al. COVID-19 pneumonia: different respiratory treatment for different phenotypes? . Intensive Care Med. 2020. |
| Gattinoni L, Coppola S, Cressoni M, Busana M, Chiumello D. Covid-19 Does Not Lead to a ”Typical” Acute Respiratory Distress Syndrome. Am J Respir Crit Care Med. 2020. |
| Ziehr DR, Alladina J, Petri CR, Maley JH, Moskowitz A, Medoff BD, et al. Respiratory Pathophysiology of Mechanically Ventilated Patients with COVID-19: A Cohort Study. Am J Respir Crit Care Med. 2020;201(12):1560-4. |
| Ferrando C, Suarez-Sipmann F, Mellado-Artigas R, Hernandez M, Gea A, Arruti E, et al. Clinical features, ventilatory management, and outcome of ARDS caused by COVID-19 are similar to other causes of ARDS. |
| Intensive Care Med. 2020. Tobin MJ. Basing Respiratory Management of COVID-19 on Physiological Principles. Am J Respir Crit Care Med. 2020;201(11):1319-20. |
| Grieco DL, Bongiovanni F, Chen L, Menga LS, Cutuli SL, Pintaudi G, et al. Respiratory physiology of COVID-19-induced respiratory failure compared to ARDS of other etiologies. Crit Care. 2020;24(1):529. |
| Raoof S, Nava S, Carpati C, Hill NS. High-Flow, Noninvasive Ventilation and Awake (Nonintubation) Proning in Patients With Coronavirus Disease 2019 With Respiratory Failure. Chest. 2020. |
| Camporota L, Sanderson B, Dixon A, Vasques F, Jones A, Shankar-Hari M. Outcomes in mechanically ventilated patients with hypoxaemic respiratory failure caused by COVID-19. Br J Anaesth. 2020. |
| Marini JJ, Dellinger RP, Brodie D. Integrating the evidence: confronting the COVID-19 elephant. Intensive Care Med. 2020;46(10):1904-7. |
| Fan E, Beitler JR, Brochard L, Calfee CS, Ferguson ND, Slutsky AS, et al. COVID-19-associated acute respiratory distress syndrome: is a different approach to management warranted? Lancet Respir Med. 2020;8(8):816-21. |
| Suffredini DA, Allison MG. A Rationale for Use of High Flow Nasal Cannula for Select Patients With Suspected or Confirmed Severe Acute Respiratory Syndrome Coronavirus-2 Infection. J Intensive Care Med. 2020:885066620956630. |
| Grasselli G, Tonetti T, Protti A, Langer T, Girardis M, Bellani G, et al. Pathophysiology of COVID-19-associated acute respiratory distress syndrome: a multicentre prospective observational study. Lancet Respir Med. 2020. |
| Coppo A, Bellani G, Winterton D, Di Pierro M, Soria A, Faverio P, et al. Feasibility and physiological effects of prone positioning in non-intubated patients with acute respiratory failure due to COVID-19 (PRON-COVID): a prospective cohort study. Lancet Respir Med. 2020;8(8):765-74. |
| Tobin MJ, Laghi F, Jubran A. Why COVID-19 Silent Hypoxemia Is Baffling to Physicians. Am J Respir Crit Care Med. 2020;202(3):356-60. |
| Larsson E, Brattstrom O, Agvald-Ohman C, Grip J, Campoccia Jalde F, Stralin K, et al. Characteristics and outcomes of patients with COVID-19 admitted to ICU in a tertiary hospital in Stockholm, Sweden. Acta Anaesthesiol Scand. 2020. |
| Paul V, Patel S, Royse M, Odish M, Malhotra A, Koenig S. Proning in Non-Intubated (PINI) in Times of COVID-19: Case Series and a Review. J Intensive Care Med. 2020;35(8):818-24. |
Finjusteringar i respiratorn
Det gäller att komma ihåg att normal andning hos människan är ett fysiologiskt mästerverk. En stor diffusionsyta i lungorna i ett relativt sett litet hålrum samverkar dels med en effektiv muskelmotor dels med blodgenomströmningen i lilla kretsloppet. Kombinationen reglerar i huvudsak oxygenering samt elimination av koldioxid. Andningen styrs centralt av efferenta och afferenta neurofysiologiska banor som kan reagera och justera andningen momentant efter behov. Ventilation och perfusion utgör ett finstämt system som är resultatet av en evolution under miljontals år. Ventilation i respiratorn är däremot inte det utan beror helt på våra inställningar i en mekanisk respirator under övertrycksventilation. Ventilatorbehandling idag är i bästa fall en ganska klumpig imitation av naturlig andning, även om den utgör fundamentet för modern intensivvård.
I det enklaste fallet vid volymkontrollerad ventilation (VK), där patienten inte bidrar med egen andning, säkerställer respiratorn syresättning och koldioxidelimination med bibehållen volym men med varierande insufflationstryck. Respiratorbehandling innebär övertrycksventilation av lungorna medan normal andning är en form av undertrycksventilation. Det är övertrycket som på olika vis skadar lungorna vid långvarig respiratorbehandling. Målet med modern ventilatorbehandling är därför att begränsa ventilatorinducerad lungskada (VILI) samt att förhindra att patienten skadar sig själv genom prolongerat ökat andningsarbete (”patient self-inflicted lung injury, P-SILI”). En begränsning av lungskadan är endast möjlig så länge vi håller oss inom säkerhetsmarginalerna beträffande tidalvolym, topptryck och transpulmonellt drivtryck.
Under assisterad ventilation (ASB/TU/CPAP) styr patienten sin andning själv, vilket kräver ökad uppmärksamhet och anpassning av respiratorinställningar till ett individuellt och dynamiskt behov. Den mest använda formen av assisterad ventilation är sannolikt tryckunderstödd ventilation, så kallad TU/CPAP. Andra assisterade ventilatonsmodus såsom NAVA, APRV, PAV finns tillgängligt men används i mindre utsträckning. Däremot kommer de flesta av alla IVA-patienter med en respiratortid över ett dygn att tillbringa en del av sin urträningsfas i TU/CPAP.
Justerbara parametrar i TU/CPAP
- Triggerkänslighet
- PEEP
- Tryckunderstöd (= tryck över PEEP)
- Inspirationsstigtid (inspiratory rise)
- Inspirationsavslut (cycling off)
TK (tryckkontrollerade andetag) ligger alltid som backup mode under TU/CPAP. Denna andningsfunktion tar över med kontrollerade andetag när inga andningsförsök görs under en förinställd apnétid.
Tryckunderstödd ventilation (TU)
Den inspiratoriska stigtiden (inspiratory rise time) definierar tiden från att andetaget utlösts till maximal inandningsflöde uppnås. Inspirationsavslut (cycling-off airflow threshold) beskriver punkten där inandning övergår till utandning som procentandel av maximalt inandningsflöde.

Triggerkänslighet
Om hur ett andetag utlöses: I TU/CPAP använder sig respiratorn av en pneumatisk trigger som antingen är flödes- eller tryckbaserad. Under flödesbaserad triggning känner respiratorn av ett inandningsförsök genom en uppmätt reversering i utandningsflödet. För att kunna registrera och framförallt mäta reverseringen använder respiratorn sig av ett så kallad bias-flöde. Det betyder att respiratorn under utandning tillför ett luftflöde på 2 l/min som löper parallellt med exspirationsflödet. Detta för att få en konstant ”baseline” som är mätbar och som varken är individuell eller varierande som en fysiologisk utandning. När patienten initierar ett andetag minskas detta bias-flöde relativt till patientens inspiration. Förändringen i luftflödet som sker utlöser ett assisterat andetag när det passerar det förinställda trigger-värdet. En lagom default inställning i TU/CPAP skulle kunna vara 1,4 l/min. Ett sänkt värde innebär en ökad känslighet samt en snabbare responstid som kan öka patientkomforten, patienten kan därigenom lättare trigga varje andetag. Man bör vara medveten om risken för auto-triggning vid väldigt låg triggerkänslighet, genom t.ex. rörelser eller läckage i andningscirkeln, vilken ökar ju mer vi sänker tröskeln. Detta kan skapa ett dyssynkront andningsmönster som i sin tur, utöver att stressa patienten, även ökar risken för ventilatorinducerad lungskada.
Vid tryckbaserad trigger initieras ett andetag när patienten genom ett inandningsförsök skapar ett undertryck under det förinställda PEEP-värdet. Principen är ”enkel” och fungerar i de flesta respiratorer. Nackdelen är att det oftast ökar respiratorns responstid och kan vara belastande för patienten med ökat andningsarbete, jämfört med flödesbaserad triggning. Risken för självutlösande andetag verkar vara mindre i tryckbaserad triggerinställning även med lågt tröskelvärde. Däremot kan man med ett högt triggervärde verkligen utmana patienten eller rentav förhindra att andetagen triggas överhuvudtaget. För högt inställd trigger försvårar spontanandningen och kan därigenom upplevas som obehagligt för patienten.
Det finns väldigt få vetenskapliga studier av olika trigger-inställningar värderat mot kliniska utfallsmått. Flödesbaserad triggning förefaller vara en modernare och smartare variant. Rekommendationen skulle således kunna vara att inte ändra på den förinställda flödes-triggern om det inte finns ett kliniskt uppenbart triggningsproblem.
PEEP
Grundtanken för inställningen av PEEP är enkel, att alltid behålla ett intra-alveolärt tryck över noll cm H20 för att förhindra end-expiratorisk kollaps av lungvävnaden. Målet är, hypotetiskt sett, en global (= i hela lungan), konstant (= över hela andningscykeln) och persisterande (över hela behandlingsperioden) ventilations/perfusionskvot (V/Q) som ligger så nära ett som möjligt. Det handlar således om att hitta rätt PEEP-nivå som varken är för låg eller för hög, ett så kallat optimalt PEEP.
Ett för lågt PEEP kan öka risken för shuntutveckling, dynamisk ”recruitment/derecruitment” som leder till ”shearing stress” och atelektatiskt trauma som i sin tur ökar risken för lungskada och ARDS utveckling. Ett för högt PEEP kan öka risken för endtidal överdistension av lungorna med ökat dead-space som i sin tur kan skapa ett behov av ökat drivtryck (> 15-20 cm H2O). Den bästa metoden för att hitta rätt PEEP-nivå under kontrollerad ventilation är omdiskuterad, inga konklusiva data finns ännu. Flera metoder är dessutom relativt krångliga i praktiken.
Ett grundläggande problem med all PEEP-metodik är att en momentan förbättring i lungmekanik eller gasutbyte inte nödvändigtvis innebär en förbättring över tid. Gällande ventilatorinducerad lungskada och ARDS kan nyttan eller skadan av en given förändring ibland bedömas först efter flera dagars behandling. Man bör även komma ihåg att alla tryck som mäts i samband med respiratorbehandling mäts som globala mått. Patientens lunga däremot utsättas dels för olika tryck i olika delar samtidigt som elasticitet, eftergivlighet och atelektasbenägenhet också varierar i olika delar av lungan.
Det som tillkommer under assisterad ventilation är att inspirationstrycket som lungan egentligen utsätts för, det transpulmonella trycket, ännu inte kan mätas på ett enkelt sätt men metodutveckling pågår. Dessutom är den understödda ventilationen patientstyrd och därmed varierande i både volym och dynamik. Detta försvarar eller gör det rentav omöjligt att dra slutsatser av de flesta mätmetoder som har använts bedside. När det gäller PEEP och TU/CPAP har vi med andra ord relativt liten nytta av att mäta:
- Statisk compliance
- Lowest infliction point
- Lowest shunt
- Lowest deadspace fraction
Trots att manometri med esofagusballong förefaller vara en bra metod för att mäta transpulmonellt tryck med stor klinisk potential för att kunna styra respiratorbehandlingen så verkar den inte ha någon rutinmässig plats för att hitta rätt PEEP-nivå under assisterad ventilation.
Elektrisk impendans tomografi (EIT) ter sig som en praktiskt mer lovande och användbar metod när det gäller PEEP-justering, både i kontrollerad och assisterad ventilation. Men trots att tekniken i sig inte är ny samt att den har använts framgångsrikt i flera kliniska studier ligger den än så länge långt ifrån en rutinmässig användning.
Sammanfattningsvis finns det, gällande PEEP, inte så mycket konkret vetenskap som skulle kunna hjälpa oss att hitta rätt nivå. Som vägledning kan man i klinisk praxis studera trendbilden på respiratorn med förändringar i dynamisk compliance under det senaste dygnet. T ex kan återkommande försämringar som kan relateras till vändningar av, en för övrigt smärtfri och ostressad patient, stå för en ökad atelektasbenägenhet. Patienten skulle då med största sannolikhet må bra av ökad PEEP. Vid låg dynamisk compliance med krav på ett högt drivtryck för att åstadkomma adekvata tidalvolymer, samt en patient som behöver använda accessoriska andningsmuskler, kan eventuellt en sänkning av PEEP leda till omedelbar förbättring. Oavsett åt vilket håll vi justerar PEEP bör vi följa och utvärdera förändringar av dynamiska andningsmått över tid tillsammans med den kliniska bilden.
Tryckunderstöd
Vid övergång från tryckkontrollerad ventilation (alternativt VKTS) till tryckunderstödd ventilation kan understödsnivån (TU över PEEP, ”drivtrycket”) oftast reduceras. Detta då patienten ifråga börjar bidra till andningen själv genom diafragmakontraktion. I tryckunderstödd ventilation är trycket under inspirationsfasen konstant samtidigt som flödet avtar. Så länge TU är satt på ett värde där patienten inte är ”tryckunderstödsberoende” kan patienten bestämma sin tidalvolym (VT) själv. Underskrider vi däremot värdet till en nivå där patienten inte längre kan kompensera genom egen ansträngning kommer VT att minska i förhållande till tryckunderstödet.
Som generella mål för justering av TU bör man eftersträva en andningsfrekvens under 30/min och en tidalvolym under 6 ml/kg (IBW). Vidare bör man eftersträva en andning utan auxillär andningsmuskulatur med en ”lugn” och ostressad patient. Bedömningen av sista punkten är givetvis svår, då det i regel finns mycket annat utöver respiratorbehandlingen som kan stressa patienten.
Urträning ur respiratorn – ”weaning”
Under urträning bör man hålla tryckunderstödet under 20 cm H2O. Beträffande understödsnivån (där vi uppnår adekvata tidalvolymer) är det nödvändigtvis inte den nivå som patienten måste ha. Målet under urträning kan vara maximal träningseffekt med minimal ansträngning. En protokollstyrd urträning med strukturerad nedtrappning av support och till slut extubation har i litteraturen visat sig ge fler respiratorfria dager. Eftersom respiratorbehandling och urträning oftast styrs av läkare på basen av individuella beslut saknas standardiserade urträningsprotokoll på de flesta kliniker i landet. Ett pragmatiskt råd är att man regelbundet, utvärderar och ev. sänker TU tills patienten behöver öka sitt andningsarbete. Tecken på detta kan vara en ökad andningsfrekvens eller en synlig insats av auxiliär andningsmuskulatur, oftast tydligast i m. sternocleidomastoideus. Ett annat bra sätt är givetvis att prata med patienten, som i urträningsfasen oftast är kommunicerbar, och be vederbörande signalera när det börjar kännas för jobbigt med andningen. Understödsnivån vi väljer ligger snäppet över ansträngningströskeln. Patienten skall dock aldrig ”slita ont” i respiratorn och riskera att bli utmattad. Extubation av en uttröttad patient är kontraindicerat. Acceptans av 5 över 5 i understödstryck/PEEP med FiO2 under 0,3 anses som ett säkert mått att extubera ifrån. Även högre trycknivåer kan gå att extubera ifrån i vissa fall. Det är alltid en klar fördel om patienten är kommunicerbar och lugn under extubationen. Man bör undvika ”crash extubation”.
Stigtid
Det inställda trycket eller luftflödet som assisterar patienten under inandningen (tryck över PEEP i TU/CPAP mode) är inte maximalt från början utan ökar successivt efter att andetaget har utlösts. Ökningens hastighet ställs in med inspiratorisk stigtid (inspiratory rise time).
Tryckunderstödd ventilation (TU)
En förkortning av den inspiratoriska stigtiden (A+B) leder till en minskad inspirationstid utan större förändring av tidalvolymen (VT) genom en vänsterförskjutning av inspirationskurvan. Ett ökat inspirationsavslut (C+D) minskar både inandningstiden och VT genom tidigare ”cycling-off”.

Default inställning av stigtiden i TU/CPAP är 0,15 sek. En minskning i inställd inspiratorisk stigtid påverkar, åtminstone i teorin, inte tidalvolymen. Detta är bara ”i teorin” eftersom en inadekvat förkortning av stigtiden kan leda till att inflödet avbryts i förtid med sporadiska dubbla andetag som följd (”double triggering”). Detta uppkommer pga. För hög resistens i andningscirkeln orsakat av sekret eller att patienten ”spänner emot” (”flow in excess of demand”, se kurva A nedan).
Dubbla andetag behöver inte nödvändigtvis uttrycka ett krav på ökad inspiratorisk stigtid utan måste alltid relateras till den kliniska situationen. En förlängning av inspiratorisk stigtid kan vara fördelaktigt hos en ARDS-sjuk patient med atelektastendens eftersom det skapar tid för en adekvat omfördelning av tidalvolym mellan alveoler med olika tidskonstanter. För lång stigtid däremot kan leda till en känsla av andnöd och ökat andningsarbete. Detta kan bli synligt genom en konkav deflektion av den inspiratoriska tryckkurvan (kurva C nedan).
Exempel på dyssynkroni pga. inadekvat inspiratorisk stigtid. (A) i figuren visar kort inspiratorisk stigtid (0,0 sek) med tidig trycktopp under inspirationsfasen som tecken på ”flow in excess of demand” alternativt obstruktion i luftvägarna eller i tuben. (B) visar normal inandningskurva. (C) visar lång inspiratorisk stigtid (0,5 sek) med konkav deformering av kurvan under flödesökning som tecken på ”demand in excess of flow” med konsekutivt ökat andningsarbete.

Generellt sett skulle man kunna säga att en kort inspiratorisk stigtid (förkortad inandning i relation till utandningstid) gynnar framförallt den obstruktiva patienten (astma, KOL), samt att en förlängning ibland med fördel kan användas för patienter med atelektastendens vid långsam andningsfrekvens.
Inspirationsavslut
Luftflödet under inandningen börjar avta så fort den förinställda trycknivån har uppnåtts. När flödet understiger en viss nivå som uttrycks i procent av maxflödet så övergår inspirationen till expiration (eng: ”cycling off”). Det förinställda värdet är 30 %. Ökar vi värdet genom att förändra inspirationsavslutet så förkortas patientens andetag och vice versa.
Ökat inspirationsavslut till 50% (C) med konsekutivt minskad tidalvolym (VT). Bild (D) visar försök till VT kompensation genom minskning av inspirationsavslut till 30% samt förkortad inspiratorisk stigtid till 0,0 sek.

Syftet är uppenbart att påverka I:E förhållandet. Att ge den obstruktiva patienten mer tid för att andas ut och minska risken för auto-PEEP (ökat inspirationsavslut, gärna i kombination med förkortad inspiratorisk stigtid) eller öka inspirationstiden för den atelektasbenägna restriktiva patienten med låg compliance (sänkt inspirationsavslut med eventuell förlängning av inspiratorisk stigtid). Dubbla andetag kan uttrycka ett behov av ytterligare sänkning av inspirationsavslutet.
Sammanfattningsvis
Finjusteringar i respiratorinställningarna tillåter oss att optimera respiratorbehandlingen för den enskilda patienten. Även om det finns alternativ till TU/CPAP så kan detta andningsmodus generellt anses vara det mest effektiva urträningsmönstret. Default-inställningar i TU/CPAP bör vara basen i respiratorinställningen men justeringar kan krävas mot bakgrund av den specifika lungpatologin och variera under urträningens olika faser. För att nå en effektiv urträning ur respiratorbehandlingen krävs aktiv närvaro med relevanta justeringar av respiratorinställningar och viss acceptans av ”trial and error”-principen under beaktande av lungfysiologiska principer och kontinuerlig monitorering av respirationen och patientens samlade kliniska bild.
Flera olika mätmetoder finns för att hitta optimala respiratorinställningar men basal klinisk undersökning kompletterat med ultraljudsundersökning, täta blodgasanalyser samt vanlig slätröntgen är oftast tillräckligt för att kunna optimera ventilationen. Datortomografi eller magnetkameraundersökning ökar i vissa fall med restriktiva inslag ytterligare förståelsen för patientens lungsjukdom och bör utföras relativt liberalt på intensivvårsdpatienter.
Urträning ur respirator – praktiska råd
Aktiv urträning rekommenderas endast på dagtid mellan 07-22
Kriterier för uppstart av aktiv urträning
- Parametrar inom målordinationerna och kliniskt stabil patient
- TU/CPAP senaste 12 h, FIO2 ≤ 50%, PEEP ≤ 15, TU ≤ 20, stabila blodgaser
- Stabil cirkulation med minskat/oförändrat inotropt stöd
- Sjunkande infektionsparametrar
- Temp < 38,5 gr
- Ej för stor kumulativ plusbalans
- Magen igång
- Kontrollerad smärta – låga doser opiater
- RASS -3 eller högre
PEEP
- Reducera PEEP med 2 cm varannan timme (max 6 ggr/dygn) tills PEEP är nere på 5-8 och justera syrgasen utifrån behov
- Om FIO2 > 40% bevara PEEP ≥ 10
Tryckunderstöd
- Reducera TU med 2 var fjärde timme, så länge TV är över 6 ml/kg (max 4 ggr/dygn) tills TU är 8
- Blodgas tas före ny ändring samt 30 min efter
Om patienten visar tecken på
- Stress/oro
- Smärtpåverkan
- Avvikande värden utifrån målordinationer
- Stigande andningsfrekvens > 30
Överväg åtgärder
- Vid respiratoriska försämringar så återgå till föregående respiratorinställningar
- Överväg andra orsaker än respiratoriska
Kriterier för extubation
- Vaken patient
- Kan krama händerna på uppmaning
- Kan ge ögonkontakt
- Adekvat hostreflex
- Ej mycket slem
- Om PEEP 8 och syrgas 35 % så kan patienten extuberas men patienten kommer att behöva NIV
- Om PEEP 5 och syrgas 25 % förväntas patienten klara sin andning med 1-2 L syrgas på grimma
Urträning vid tracheostomi
Patient med tracheostomi Följ urträningen ovan, fortsätt sedan med punkterna A-G enligt nedan, helst ett dygn per steg
A. Utan ventilator 5 min varje timme, tiden ökas succesivt till 15 min. Nattetid TU/CPAP
B. Utan ventilator 20 min varannan timme, tiden ökas succesivt till 40 min. Nattetid TU/CPAP
C. Utan ventilator 40 min varannan timme, öka till 60 min. Försök med talventil. Nattetid TU/CPAP
D. Utan ventilator 60 min varannan timme, öka till 90 min. Försök med talventil. Nattetid TU/CPAP
E. Utan ventilator dagtid förutom inhalationer, som ska ges minst x 4*. Nattetid TU/CPAP
F. Hela dygnet (även nattetid) utan respirator förutom inhalationer, som ska ges minst x 4*
G. När patienten bedöms ha en fullgod egen andning överväg dekanylering, som bör ske under förmiddagen
* Finns inte inhalationer ordinerade så ordinera in 4 ml NaCl x 4 dagtid som inhalation
Kriterier för dekanylering
- Har klarat ett helt dygn utan respiratorstöd, förutom inhalationer
- Bedöms inte ha en pågående klinisk försämring
- Bedöms ha bevarad svalgfunktion och kunna hålla fri luftväg
- Bedöms ha passage av luft från trachea genom att kunna andas förbi trachealkanylen och prata
Lungrekrytering
Dessa manövrar är sällan effektiva senare än 48 timmar efter debuten av ARDS och kan då även ge allvarliga skador. Vid all lungrekrytering skall cirkulation och pulsoximetrisk saturation noggrant övervakas. Lungrekrytering har bäst effekt tidigt i förloppet av luftvägskollaps och utveckling av akut lungsvikt.
Metod 1
Insufflera en luftsyrgasblandning i lungan till ett luftvägstryck av 40–50 cm H2O under 20–30 sekunder. Fortsätt därefter att ventilera på vanligt sätt, men behåll initialt ett PEEP på 15–20 cm H2O. Manövern kan upprepas igen efter några minuter om syresättningen inte förbättrats. Under och efter insufflation, använd en så låg syrgashalt i andningsluften som möjligt för att minimera utvecklingen av absorptionsatelektaser. PEEP-nivån kan sedan sakta reduceras om den arteriella saturationen upprätthålls. Ovanstående kan antingen åstadkommas genom att låta respiratorn långvarigt insufflera lungan genom att sätta respiratorn på CPAP-andning (kontinuerligt positivt luftvägstryck) med ett totalt tryck på 40–50 cm H2O, eller genom att förlänga inspirationstiden under tryckkontrollerad ventilation och ställa in respiratorn så att det totala topptrycket blir 40–50 cm H2O. Man kan också manuellt utföra samma manöver med hjälp av en andningsballong med inkopplad manometer. Det är extremt viktigt att luftvägstrycket upprätthålls på minst PEEP-nivån efter manövern och inte tillåts komma ner på noll eller bli negativt. Undvik därför om möjligt sugning av luftvägen i detta skede.
Metod 2
Lungorna insuffleras frekvent till ett luftvägstryck på 40–50 cm H2O under en period på 5–10 minuter. Detta åstadkommer man genom att ställa respiratorn på en låg andningsfrekvens (10/min), en lång inspirationstid (50 procent), ett PEEP på 20 cm H2O och ett totalt topptryck (inklusive PEEP) på 40–50 cm H2O samt ventilera med dessa inställningar under 5–10 minuter. Därefter ställs respiratorn på de inställningar som är anvisade under metod 1.
Extubation
Extubation är avlägsnandet av endotrakealtuben som utförs efter anestesi eller intensivvård med intubation och respiratorbehandling. Tuben avlägsnas när patienten kan andas själv tillfredställande utan att bli utmattad och utan risk för desaturation. Extubation av en uttröttad patient är kontraindicerat. Acceptans av 5 över 5 i understödstryck/PEEP med FiO2 under 0,3 anses som ett säkert mått att extubera ifrån. Även högre trycknivåer kan gå att extubera ifrån i vissa fall. Det är alltid en klar fördel om patienten är kommunicerbar och lugn under extubationen. Man bör undvika ”crash extubation”.
Kriterier för extubation
- Spontan ögonöppning
- Ansiktsgrimas
- Patientrörelse annan än hosta
- Konjugerad blick
- Målmedvetna rörelser
- Endtidala nivåer av anestesigas lägre än:
- Sevofluran: 0,2%
- Isofluran: 0,15%
- Desfluran: 1,0%
- Syremättnad högre än 97%
- Positivt larynxstimuleringstest
- Endtidal volym större än 5 ml/kg
Värdera patientens förmåga till spontanandning före extubation
- Kan patienten ha understödd ventilation i respiratorn?
- Föreligger godtagbara värden på TU, PEEP 10, FiO2 <40%?
- Finns blodgaser med SaO2>95%, PaO2>10 kPa, PaCO2<6 kPa?
- Minska till extubationsinställningar med PEEP 5-7 och TU 5-7
Extubationskriterier
- Vakenhet RLS <3?
- Svalgfunktion, hostkraft?
- Klarar PEEP 5-7 och TU 5-7 eller fritt på näsa > 30 min?
- Förväntat fri luftväg efter extubation?
Utvärdering efter extubation
- Puls, blodtryck, andningsfrekvens, blodgaser?
- Inom individuellt uppsatta gränser?
- Tänkvärt: En pilot måste planera både start (intubation) och landning (extubation).
- Extubationen är alltid elektiv (om ej accidentell).
- 23 % av allvarliga luftvägsrelaterade händelser sker vid extubationen.
- De vanligaste komplikationerna vid extubation är: hypertension, takykardi, höjt intrakraniellt och intraokulärt tryck etc.
- Vanliga problem: Inadekvat oxygenering och ventilation. Oförmåga att skydda luftvägarna och få upp slem ur luftvägarna.
- Vid extubation måste man beakta att extubationen kan misslyckas.
- Vid extubation måste man bedöma om reintubation kan vara lätt eller svår.
- Reintubation under optimala förhållanden skiljer sig mycket från akut reintubation med hypoxisk patient.
- Överväg fördröjd extubation.
- Överväg extubation över en ”Airway exchange catheter”. Förbehandla med inhalation av lidokain.
När man skall ge patienter anestesi kan man många gånger välja mellan generell anestesi eller alternativt någon typ av regionalblockad, central eller perifer i kombination med sedering för det kirurgiska ingreppet. Det kan kännas lockande att till patienter med svåra luftvägar välja regionalanestesi, men då ”måste” man välja en variant som ”säkert fungerar”, t.ex. spinalanestesi. Om en blockad slutar verka under op. och man akut tvingas söva en patient med svår luftväg kan man snabbt hamna i allvarliga problem.
Hosta – vid respiratorbehandling
Svår ihållande hosta kan vara ett allvarligt problem vid behandling av intensivvårdspatienter i respirator och under urträning. Svår hosta ses bla. vid:
- ARDS
- Nylagd tracheostomi
- Covid 19 infektion
- Kikhosta (även tidigare kikhosta)
- Sarcoidos
- KOL
- Restriktiva lungsjukdomar – lungfibros
- Tracheomalaci
- RS-virus pneumoni
- Lymfom
Svår hosta på patient i respirator kan på försök behandlas med inhalation i nebulisator (x 3-6) av :
- Lidokain (Xylocain) 10 mg/ml, 1 ml +
- Bupivacain 5 mg/ml, 1 ml +
- NaCl 1 ml (totalt 3 ml), i nebulisator
Denna behandling kan ge fin hostdämpning under ett par timmar. Kan ges 3 till 6 gånger dagligen. Man kan även prova injektion av lidokain (Xylocain) 50 mg intravenöst inför mobilisering med gott resultat. Opiater givet intravenöst ger också viss hostdämpning. Vid bronkospasm och hosta kan man även pröva ett s.k. astmadropp som ges under 12 timmar :
- Glukos 5% 1000 ml +
- Teofyllamin (23 mg/ml) 20 ml +
- Betapred 4 mg
HFNC – högflödesgrimma – Optiflow
Optiflow (HFNC) är en typ av andningsunderstöd till patienter med spontanandning som medger uppluftning av luftvägarna med motståndsandning utan tättslutande mask. Optiflow ger därför många gånger bättre komfort och mindre ansträngning för patienten jämfört med CPAP i tättslutande mask. Optiflow använder sig av syrgas i ett mycket högt luftflöde, 20-60 L/min med aktiv anfuktning (NHF – nasal high flow). Systemet kan kopplas antingen via näsgrimma eller trachealkoppling. Den möjliggör behaglig och effektiv tillförsel av upp till 100 % inandad syrgas.
Bakgrund
Högt syrgasbehov innebär nästan alltid uttorkade luftvägar och sämre sekrettransport. Aktiv befuktning av syrgasflödet kan användas vid spontanandning när behovet av syrgas är högt men behov av övertryck med CPAP eller NIV inte föreligger. Aktiv befuktning möjliggör alltså höga inandade syrgaskoncentrationer utan uttorkning av luftvägarna. Gasflöde högre än 20 liter/minut skapar dessutom ett visst positivt luftvägstryck (lågt), samt en utvädring av utandad gas från näsa/svalg vilket minimerar återinandning av koldioxid. Önskad syrgashalt regleras med gasmixern.
Indikationer
Metoden kan användas istället för syrgasmask då man vill undvika uttorkning av övre luftvägar. Exempel i samband med växling mellan NIV och mask eller vid långvarigt behov av syrgas. Gasflöden upp till 35 liter/minut kan prövas utan läkarordination. Högre flöden används bara efter godkännande av ansvarig läkare. Urträning ur non-invasiv respiratorbehandling kan gå lika bra med Optiflow som med tättslutande mask (NIV).
Kontraindikationer
- Medvetslöshet
- Koldioxidretention
- Skallbasfraktur
- Likvorré
- Näsfraktur
- Näsblod i anamnesen
- Trombocytopeni < 85
- Nasala förträngningar
- Nyligen genomgången operation i näsregionen
Praktiska anvisningar
Material
- Mixer/flödesmätare
- Befuktare Fisher & Paykel
- Slangset med slang och fuktkammare
- Gasanslutning till fuktkammaren
- Sterilt vatten
- Optiflow näsgrimma
- Optiflow trachealkoppling
Optiflow via näsgrimma
- Koppla mixer/flödesmätare till luft och syrgasuttag.
- Ta fram slangset och koppla fuktkammare till sterilt vatten.
- Sätt blå andningsslang på ena utgången på fuktkammaren och adaptern på den andra. Gulmärkt kabel värmer nu endast inspirationsslangen. Blåmärkt kabel mäter temperaturen i inspirationsslangen.
- Sätt på befuktaren
- Befuktaren ska stå på invasiv ventilation, den kan inte ställas in på någon exakt grad utan justeras automatiskt; behållaren 35,5 – 42o, luftväg 35 – 40o. Den varnar för låg temp, < 35,5o, respektive hög temp, > 41o.
- Ställ in önskad syrgashalt (FiO2) på mixern.
- Flödet från mixern skall vara minst 20 liter/minut för att ge rätt syrgaskoncentration. Maximalt flöde som kan ställa in är 60 l/minut. Målet med det höga flödet är att överträffa patientens inandningsflöde och därför skapa en minimal utspädning med rumsluft. På så vis kommer patienten att få den inställda syrgasmängden
- Anslut Optiflow näsgrimma/Optiflow trachealkoppling till den blå befuktarslangen och koppla till patient. Öka gärna gasflödet gradvis vid uppstart tills befuktaren har närmat sig arbetstemperatur.

Optiflow via trachealkoppling
Aktiv befuktning via Optiflow trakealkoppling med högt flöde är ett bra alternativ till patienter med trakeostomi som intermittent spontanandas, t ex vid ventilatorurträning.
Den blå koppen är skålformad för att kunna fånga upphostat sekret. Kan tas bort och rengöras med sterilt vatten. Systemet kopplas upp på samma sätt som beskrivits ovan.
Talventil
Patient som har talventil får en ytterst begränsad möjlighet att befukta andningsvägarna. Genom att koppla på Optiflow näsgrimma under den tid talventilen används så kan patienten få en bra befuktning med syrgas. Man kan således avstå från att koppla syrgas via talventilen.
Byte/rengöring
Påse med sterilt vatten bytes 1 gång per dygn. Slangar/grimma/ trachealkoppling är enpatients och byts en gång per vecka. Rengöring av grimma vid behov med sterilt vatten.
Felsökning
Om befuktaren inte kommer upp i inställd temperatur, töm ut ev. kondensvatten vid tempprober och kontrollera att slangarna är varma. Se till att tempproben är isatt uppifrån och ordentligt nedtryckt!
Lysdioder visar vad som utlöst ev. larm. Tips: håll in befuktarens ”tysta larm”-knapp för att läsa av temp på flera mätpunkter.
CPAP – Continuous Positive Airway Pressure
Ökad motståndsandning. Förutsätter spontanandning och att patienten triggar varje andetag. Kan göras med patienten i respirator eller med en sluten andningsmask med tryckventil. Kan kombineras med tryckunderstödda andetag i ett BiPAP-system eller CPAP med ASB. Ett tryck utöver det atmosfäriska bibehålls under hela andningscykeln (exspiration + inspiration + paustid). CPAP underlättar inandning men försvårar utandning. Begreppet CPAP (Continuous Positive Airway Pressure) används vanligtvis för patienter som spontanandas.

CPAP-systemet ger höga luftflöden (80-100 l/min) med ett konstant tryck och flöde via maskventilation. Systemet kan i viss mån kompensera för förluster vid maskandning som är otät. Ger rekrytering av lungvävnaden och ökar syresättningen. Används främst vid bibehållen andningskraft vid lungödem eller atelektaser. CPAP kan vara farligt vid otillräcklig andningskraft. Fördelen är att luftvägen hålls öppen och att FRC ökar vilket underlättar andningen. CPAP är påfrestande för patienten i långa loppet och tröttar ut patienten. Vid pneumonier kan det leda till andningskollaps. Effektivt mot lungödem.
Kontinuerligt positivt luftvägstryck (Continous Positive Airway Pressure), CPAP)
- Initieras av patienten och fungerar på exakt samma sätt som TU, förutom att tryckunderstödsnivån ställs in på noll
- Upprätthåller ett positivt tryck i luftvägarna hela tiden
- Är i praktiken en spontan andningsmetod med kontinuerligt positivt tryck för att hålla luftvägarna öppna
CPAP inställningar
| Normala inställningar i CPAP | |
|---|---|
| CPAP-nivå | 3-10 cm H2O |
| AF | Varierande |
| FiO2 | 30-100% |
PEEP – Positive End-Expiratory Pressure
Ökat motstånd i utandningen på intuberad patient via en ventil i respiratorn. Upprätthåller ett positivt tryck i luftvägarna hela tiden. PEEP ger rekrytering av lungvävnaden och ökar syresättningen. Trycket i luftvägarna tillåts inte falla tillbaka till det atmosfäriska trycket vid slutet av exspirationen. PEEP används vanligen i kombination med någon av de tidigare nämnda ventilationssätten. Utgör en grundinställning i alla ventilationssätt i respiratorn. PEEP-ventilen styr utandningsventilen via servostyrning. Används främst vid lungödem eller atelektaser.
PEEP kan leda till försämrat venöst återflöde och försämrad hemodynamik med blodtrycksfall som följd. Kan även leda till ökad hjärnsvullnad och bör begränsas vid ökat intrakraniellt tryck. Bäst effekt vid extrapulmonella orsaker till andningssvikt som obesitas eller hjärtsvikt. Har bäst effekt tidigt i förloppet vid allvarlig lungsjukdom. Normala nivåer av PEEP är 5-10 cm H2O, vid ARDS kan högre motstånd behövas som 10-20 cm H2O. Har mer effekt vid diffusa infiltrat än lokaliserade. Vid höga PEEP kan lungan överdistenderas och skadas, med risk för pneumothorax i uttalade fall. Vid höga PEEP som ger stigande PCO2 överdistenderas lungan med sämre gasutbyte.
PEEP-nivå: 3-20 cm H2O.
Vanliga respiratorinställningar vid olika grader av lungskada
| Andningsfysiologiska parametrar | Frisk lunga | Måttlig lungsvikt | Svår lungsvikt |
|---|---|---|---|
| Andningsmode | TU, VK, VKTS, BiPAP | TU, VK, TK, VKTS, BiPAP | TK, (TU, VKTS), BiPAP |
| Tidalvolym ml/kg | < 6-8 | < 6-8 | < 6-8 |
| Andningsfrekvens | 15-20 | 15-20 | 15-30 |
| I:E kvot | 1:2 | 1:2-1:1 | 1:1(-2:1) |
| PEEP cm H20 | 0-5 | 5-10 | 10-20 |
| Syrgashalt % | < 40 | 40-60 | 40-100 |
| Lungrekrytering | - | Ja | Ja i tidigt skede |
ASV – Adaptive Support Ventilation
ASV står för Adaptive Support Ventilation som är ett modus i Hamiltons respirator. Adaptive Support Ventilation (ASV) upprätthåller en användardefinierad minsta minutventilation oberoende av patientens eget andningsmönster. Målet för andningsmönstret (tidalvolym och andningsfrekvens) beräknas av ventilatorn baserat på det andningsmönster som ger minst ansträngning vid andning, och att lägsta möjliga andningsarbete också ger lägst ventilatorgenererat andningstryck när det inte finns något andningsförsök från patienten.
Garanterar genom tryckstyrning en vald minutvolym. Tillåter spontanandning och anpassar ventilatorstödet efter patientens behov. Således krävs ingen ändring av andningsmode om patienten börjar/slutar trigga. Minutvolymen ställs in genom att välja ett värde på ”%MinVol”; 100 % motsvarar för
vuxna 100 ml/min/kg ideal kroppsvikt respektive för barn 200 ml/min/kg ideal kroppsvikt. Genom att välja ett annat värde än 100 % kan alltså önskat värde på minutvolym ställas in.
Startinställningar i ASV ventilation
| Patientgrupp | Idealvikt (kg) | Pinsp (cm H2O) | TI (sek) | Initial målfrekvens (b/min) | Min. Målfrekvens (b/min) |
|---|---|---|---|---|---|
| Pediatrisk patient | 15-20 | 15 | 0.8 | 20 | 10 |
| 21-23 | 15 | 0.9 | 15 | 7 | |
| 24-29 | 15 | 1 | 15 | 7 | |
| > 30 | 15 | 1 | 15 | 7 | |
| Vuxna | 30-39 | 15 | 1 | 14 | T |
| 40-59 | 15 | 1 | 12 | 6 | |
| 60-89 | 15 | 1 | 10 | 5 | |
| 90-99 | 18 | 1.5 | 10 | 5 | |
| > 100 | 20 | 1.5 | 10 | 5 |
ASV justerar inspirationstrycket och andningsfrekvensen andetag för andetag, den tar hänsyn till förändrade luftvägstryck (motstånd, compliance, RC-exp) och använder lungprotektiva inställningar för att nå målen. En minskning av tryckbegränsningen efterföljs av minskad tidalvolym (TV) och ger en ökning av frekvensen.

ASV upprätthåller en förinställd minsta minutventilation:
- Justerar automatiskt och smidigt andningsmönstret efter patientens tillstånd mellan aktiva
- och passiva andningsmönster.
- Maskingenererade andetag är tryckkontrollerade
- Spontana andetag är tryckstötta
- Förebygger takypné.
- Förebygger AutoPEEP.
- Förebygger ventilation av dead space.
- Överskrider inte ett Pinsp-tryck på 10 cmH₂O under den övre tryckgränsen.
Användaren ställer in ”Min.Vol”, ”PEEP” och ”Syrgashalt (FiO2)”. Se mer information om Att arbeta med ASV i bruksanvisningen för Hamilton Medical ventilator.
Praktisk information om att arbeta med ASV
Hamilton rekommenderar att man konfigurerar larmgränsen för ’Högt tryck’ till minst 25 cmH2O över PEEP/CPAP. Det maximala topptrycket som levereras i ASV (Pasv-gräns) är 10 cmH2O under larmgränsen.
Anslut patienten till ventilatorn och starta ASV. Respiratorn startar med tre provandetag. Ventilatorn väljer automatiskt värdena för andningsfrekvens (fTotal), inspirationstid (TI) och inandningstryck (Pinsp) baserat på beräknad IBW.
Så fort ASV startat beräknar ventilatorn ett optimalt andningsmönster och lägger till målvärden för tidvolym och frekvens i enlighet med reglerna i ASV, och specificerar ’Min.volym’ för att uppnå målen. Beroende på om patienten har passiv eller aktiv andning levererar ventilatorn volymkontrollerad eller tryckstödd andning i enlighet med en lungprotektiv strategi. Ytterligare information finns i bruksanvisningen för Hamilton Medical ventilator. Så snart de beräknade målen uppnåtts ska resultatet av ventilationen bedömas. Alla monitorerade luftvägsparametrar kan användas för detta ändamål. Men för att bedöma syra/basstatus rekommenderas att arteriella blodgaser följs kontinuerligt och att minutventilation anpassas därefter.
Exempel på justeringar under ASV ventilation
| Tillstånd | Förändring i Minutvolym |
|---|---|
| Normala arteriella blodgaser | Ingen |
| Hög PetCO₂, eller PaCO₂, | Öka 'Min.vol'. Var uppmärksam på inspirationstrycket. |
| Låg PaCO₂ | Minska "Min.volym'. Var uppmärksam på medeltrycket och syresättningsstatus. |
| Hög andningsdrive | Överväg att öka "Min.volym' Överväg sedering, analgesi eller andra behandlingar |
| Låg 0₂-mättning | Ingen. Överväg att öka PEEP/CPAP och/eller syrgashalten. |
Respiratoravvänjning från ASV
Syftet med detta avsnitt är inte att tillhandahålla klinisk information utöver vad som är nödvändigt för att använda ASV. ASV tillåter alltid patienten att andas spontant. Perioder med spontan andning kan uppstå och stöds av ASV även under en period av helt kontrollerad ventilation. Respiratoravvänjning kan med andra ord påbörjas med ASV redan innan det kan upptäckas kliniskt. Det är därför viktigt att övervaka patientens spontana andningsmönster över tid.
Progress i avvänjningen kan följas i trenddisplayen avseende inandningstryck (Pinsp), total frekvens (fTotal) och spontan frekvens (fSpont). Det kan vara nödvändigt att sänka inställningen ’Min.Volume’ till 70% eller lägre för att ”motivera” patienten att återuppta spontanandning. Om patienten kan klara flera minuter eller till och med timmar med en låg inställning för ’% Min.Vol’, Betyder det inte att avvänjningen är klar. Inställningen ’Min.volum’ måste faktiskt alltid tolkas tillsammans med nivån på ’Pinsp’, som är nödvändig för att uppnå den inställda minutventilationen. Endast om ’Pinsp’ och ’fKontrol’ har sina lägsta värden, kan det antas att avvänjningen är klar.
BiPAP – Biphasic Positive Airway Pressure
Tryckkontrollerad ventilation med utrymme för spontanandning under hela andningscykeln. Justerbart tryckunderstöd i två lägen. Man ställer in trycknivån i både CPAP-andetag och understödda andetag (ASB). BiPAP förbättrar den alveolära ventilation och ökar funktionell residualkapacitet (FRC) samtidigt som luftvägen hålls öppen. BiPAP används vid behandling av både lindrig, måttlig och svår lungsvikt.
- Är en mode med tidscykler och tryckbegränsning som medger spontan andning under hela ventilationscykeln
- Har två trycknivåer med tidscykler och växlar mellan dessa båda nivåer. Patienten kan andas spontant vid båda nivåerna och det är möjligt att ge tryckunderstöd vid båda nivåerna.
BiPAP-assist (med ASB)
Tryckkontrollerad assisterad ventilation.
BiPAP inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| TD: | 6-8 ml/kg |
| AF: | 10-20 andetag/minut |
| TU: | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP: | 5-10 cm H2O |
| FiO2: | 25-40% |
| CPAP: | 3-7 cm H2O |
| ASB: | 3-10 cm H2O |

(S)CMV+
Motsvarar VKTS med automode. Tryckkontroll med inställd tidalvolym som målvärde. Om patienten triggar levereras ett volymkontrollerat andetag motsvarande inställd tidalvolym med lägsta möjliga tryck.
APRV – Airway Pressure Release Ventilation
Spontanandning på två olika trycknivåer som regleras oberoende av varandra i egenkontrollerad respiratorandning. APRV förbättrar den alveolära ventilation och ökar funktionell residualkapacitet (FRC) samtidigt som luftvägen också hålls öppen. APRV ger CPAP på två olika nivåer vid komplett spontanandning. APRV används vid behandling av både måttlig och svår lungsvikt. APRV finns i Drägers ventilatorer som en specifik respiratorinställning (andningsmode).
- Är en mode med tidscykler och tryckbegränsning som medger spontanandning under hela ventilationscykeln.
- Alternerar mellan två nivåer av positivt luftvägstryck, med huvuddelen av tiden vid den högsta nivån och en kort utandning för att underlätta ventilationen.
- Skiljer sig från Bi-Vent genom att här används en inverterad I:E-kvot.

Förenklat är APRV ett andningsmode i respirator som tillåter spontan egenandning med ett högt CPAP-motstånd som varieras med korta trycksläpp i andningscykeln för att förbättra den totala koldioxid-eliminationen ur lungorna.
APRV kan användas som:
- ett alternativt ventilationsmode i de fall där konventionella ventilationsstrategier inte uppnått förväntad effekt
- ett möjligt alternativ till bukläge vid svår lungsvikt
- en alternativ lungrekryteringsmetod
Indikationer
- hypoxisk respiratorisk svikt (typ 1) med högt PEEP krav (≥ 12 cmH2O) och låg P/F ratio (≤ 26,7)
- lägre indikationströskel vid tydlig klinisk försämring
- potentiellt rekryterbar låg lungkompliance
- dyssynkroni i andningen med konventionella respiratorinställningar pga hög eller varierande andningsfrekvens
Kontraindikationer
Alla kontraindikationer är relativa och måste värderas omtänksamt i varje fall
- obstruktiv lungsjukdom (KOL, astma med exspiratorisk tidskonstant >0,8 s)
- högerhjärtssvikt
- allvarlig hypovolemi
- högt intrakraniellt tryck
Initiala inställningar
- Phög i flesta fall mellan 25-30 cm H2O
- som underlag kan man räkna ut medeltalet av Pmedel och Ptop av den föregående konventionella respiratorinställningen
- Plåg (markerad som ”PEEP”): 0 cm H2O eller lägsta värde som respiratorn tillåter
- Thög: 4 sek
- Tlåg: 0,4 sek
- I:E 10:1 (ska inte betraktas som fast)
- Alla TU (tryckunderstöd): 0 cm H2O

Justering av inställningar
- Utvärdera släppvolymer (den tidalvolym som mäts i släpperioderna) och justera Tlåg för att uppnå släppvolymer på 6-8 ml/kgABW. Minska Tlåg i 0,05 s steg för att minska släppvolymen eller öka Tlåg i samma steg för att få högre släppvolym.
- Innan höjning av Tlåg måste tryck- och flödeskurvan granskas för att undvika derekrytering som skulle förekomma vid för långa Tlåg Skiftet från lågt till högt tryck ska ske vid ett utandninsgflöde som motsvarar ungefär 50-75% av toppflödet. Under 50% av toppflödet tappas auto-PEEP och följaktligen ökar risken för derekrytering. Om man inte kan nå de önskade släppvolymerna utan att ha en farlig flödesminskning bör man höja Phög med 2 cm H2O per steg.
- Kontrollera en blodgas inom en halvtimme.
- Om patienten retinerar koldioxid optimera sederingen för att få bättre spontant andningsarbete. Man får minska T hög med 0,5 s steg för att höja släppningperioders frekvens. Då för att bibehålla Pmedel tänk på att höja Phög med 1-2 cmH2O steg.
- För att höja PaO2 öka Phög i 2 cm H2O steg. Om PaCO2 värde tillåter det kan man förlänga Thög också. Orimligt lång Thög (> 5 s) kommer nog inte att ge ytterligare syresättningsförbättring och samtidigt kan det vara obekvämt för patienten.
- Utvärdera patientens andningsarbete. Vid uppenbart hög andningsansträngning får man försöka minska Thög med 0,05 s steg och prova att justera P-hög (antingen minska eller höja med 2 cm H2O) för att hitta optimalt värde. Kontrollera att släppvolymerna är tillräckligt stora. Fördjupa försiktigt sederingen för att inte helt förlora den spontana andningen. Om patienten trots alla insatser kämpar mot respiratorn byt tillbaka till ett konventionellt mode.
Nedtrappning
Om det finns en förbättring i hela den kliniska bilden (FiO2 ˂ 50%, lugn spontanandning (10-25/min AF) hos en lätt sederad patient (RASS -1/-2) börjar man med att sänka Phög i steg om 2 cm H2O. Vid mindre än 20 cm H2O P hög kan man förlänga Thög med 0,5-1 s steg med 4-8 timmars mellanrum. Målet är att ta patienten nära en riktig CPAP behandling.
Teoretisk bakgrund
APRV mode skiljer sig konceptuellt från andra ventilationssätt och bygger på idén att långsamt rekrytera och hålla lungorna öppna. Det långa höga trycket låter alveolerna fyllas upp balanserat och därmed minskas heterogenitet i lungornas utfyllnad. Patientens bevarade spontana andning under P-hög förbättrar V/Q kopplingen och härmar de fysiologiska intratorakala tryckändringarna med alla sina gynnande hemodynamiska effekter. Med lägre topptryck förekommer färre iatrogena skador. Vanligtvis efter några timmars inställning med APRV brukar blodgasvärdena möjliggöra att minska FiO2 pga. långsam rekrytering, det betyder samtidigt att man måste ägna tillräckligt lång tid till patientens respiratorinställning för att få påtagliga effekter av APRV-behandlingen.
Referenser
- Fredericks AS, Bunker MP, Gliga LA, et al. Airway Pressure Release Ventilation: A Review of the Evidence, Theoretical Benefits, and Alternative Titration Strategies. Clin Med Insights Circ Respir Pulm Med. Published 2020 Feb 5.
- Farkas J IBCC chapter: Guide to APRV for COVID-19, 8 april, 2020, https://emcrit.org/pulmcrit/aprv-covid/
- van der Zee P, Gommers D. Recruitment Maneuvers and Higher PEEP, the So-Called Open Lung Concept, in Patients with ARDS. Crit Care. 2019;23(1):73. Published 2019 Mar 9.
- Jain SV, Kollisch-Singule M, Sadowitz B, et al. The 30-year evolution of airway pressure release ventilation (APRV). Intensive Care Med Exp. 2016.
- Ehab G Daoud, Hany L Farag, Robert L Chatburn: Airway Pressure Release Ventilation: What Do We Know? Respiratory Care Feb 2012, 57 (2) 282-292
APRV inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| P-hög: | 25-30 cm H2O |
| P-låg (markerad som ”PEEP”) | 0 cm H2O eller lägsta värde som respiratorn tillåter |
| T-hög: | 4 sek |
| T-låg: | 0,4 sek |
| I:E | 10:1 ska inte betraktas som fast |
| FiO2: | 25-40% |
| Alla TU (tryckunderstöd): | 0 cm H2O |
DuoPAP andningsmönster
DuoPAP är en form av ventilation, där spontanandning levereras på två alternativa CPAP-nivåer. I detta andningsmönster växlar ventilatorn regelbundet mellan två definierade trycknivåer av positivt luftvägstryck eller CPAP.
Växlingen mellan nivåerna regleras av DuoPAP tidsinställningen eller av patientens egna andetagsförsök. I DuoPAP bestäms växlingen mellan de två nivåerna utifrån tryckinställningarna (P hög) och ’PEEP/CPAP’, och tidsinställningen (T hög) och ’Frekvens’. T hög är lika med tiden med högt tryck i andningscykeln.

Observera följande:
- Med konventionella inställningar och i frånvaro av spontanandning liknar DuoPAP Pressure Control ventilation plus (PCV+).
- När frekvensen reduceras, medan ’T hög’ hålls kort jämfört med tiden för den lägre trycknivån, liknar detta andningsmönster mer PSIMV+ med spontana andetag efter kontrollerade andetag.
- Om ’T hög’ är inställd nära andningscykeltiden med tillräcklig tid på låg nivå för att tillåta full eller nästan full expiration liknar detta andningsmönster APRV.
’Pressure Support’ kan användas till att assistera spontanandning i DuoPAP, oavsett om det inträffar i ’PEEP/CPAP’- eller i ’P high’. ’Pressure Support’ ställs in ovanför ’PEEP/CPAP’, vilket betyder att spontana andetag endast understöds på ’P hög’-nivå när detta måltryck är högre än ’P high’.
IPPV – Intermittent Positive Pressure Ventilation
IPPV håller lungorna expanderade genom att konstant volym av luft blåses in. Konstant volym ges i både kontrollerat mode och assisterat. Det positiva trycket kan kontrolleras av stimulering av patientens egen spontaninspiration eller genom fullständig mekanisk ventilation. Tillgång till patientens lungor sker antingen genom intubering eller andningsmask. IPPV omfattar CPPV (continouos positive pressure ventilation), PLV (pressure limited ventilation), Auto-flow (automatisk reglering av inspirationsflödet) och IRV (inversed ratio ventilation). IPPV används främst vid behandling av lindrig eller måttlig lungsvikt.
IPPV inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| ASB | 3-12 cm H2O |
| TD (tidalvolym) | 6-8 ml/kg |
| AF (andningsfrekvens) | 10-20 andetag/minut |
| TU (tryckunderstöd) | 5-15 cm H2O |
| I:E (in-utandningsförhålllande) | 1:2 |
| PEEP | 5-10 cm H2O |
| FiO2 | 25-40% |
| CPAP | 3-15 cm H2O |
MMV – Mandatory Minute Ventilation
MMV ger spontanandning med automatisk justering av den obligatoriska andningen till patientens behov av volym. Tillgång till patientens lungor sker genom intubering eller andningsmask. Har möjlighet till PLV (pressure limited ventilation) och Auto-flow (automatisk reglering av inspirationsflödet). MMV används främst vid behandling av lindrig eller måttlig lungsvikt.
- Levererar en förinställd tidalvolym eller minutvolym under en förinställd inspirationstid och vid en förinställd andningsfrekvens, oberoende av förändringar i resistans eller compliance i lungan eller thorax
- Upprätthåller ett konstant flöde med varierande topptryck
MMV - inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| ASB: | 3-12 cm H2O |
| TD: | 6-8 ml/kg |
| AF: | 10-20 andetag/minut |
| TU: | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP: | 5-10 cm H2O |
| FiO2: | 25-40% |
| CPAP: | 3-15 cm H2O |

PCV+
Motsvarar Tryckkontroll med automode. Om patienten triggar levereras ett tryckkontrollerat andetag baserat på inställt PEEP och Pkontroll (= tryck över PEEP).
SIMV – Synchronized Intermittent Mandatory Ventilation
Delvis kontrollerad andning där patienten inte behöver andas själv. SIMV är en blandning av de kontrollerande och assisterande ventilationssätten. Ger ett garanterat förinställt antal andetag per minut. Tillåter spontanandning mellan andetagen. Under tillämpning av SIMV tillåts med andra ord både patientens understödda spontanandning och ventilatorns obligatoriska, kontrollerade andetag. De andetag som patienten själv drar ges antingen med deccelererande eller konstant flöde, dvs. volymkontrollerade eller tryckkontrollerade andetag. SIMV används främst vid urträning ur respirator och god spontanandning, oftast i en övergångsfas till spontanandning. Kan även användas till patient som inte trivs i volymkontrollerad eller tryckkontrollerad ventilation. Har möjlighet till PLV (pressure limited ventilation) och Auto-flow (automatisk reglering av inspirationsflödet). SIMV används vid behandling av både måttlig och svår lungsvikt. Används vid oregelbunden andning, vid urträning eller när patienten är på väg att ta över andningen själv. SIMV kan ställas in med understödd andning i VKTS mode eller TK mode.
- Synkroniserad intermittent obligatorisk ventilation
- Användaren ställer in hur många SIMV-andetag (obligatoriska andetag) som ska levereras varje minut
- Patienten kan andas spontant med tryckunderstöd mellan de obligatoriska andetagen
- Det spontana/tryckunderstödda andetaget definieras genom att ställa in tryckunderstödsnivån över PEEP
- Om patienten inte andas alls, levereras endast de obligatoriska andetagen
- Om patienten triggar under SIMV-perioden levereras det inställda obligatoriska andetaget. Under nästa SIMV-period väntar ventilatorn på patienttriggningen, men om detta inte har inträffat under de första 90% av andningscykeltiden (SIMV-perioden) levereras ett obligatoriskt andetag.
SIMV ASB (Assisted Spontaneous Breathing)
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| ASB: | 3-12 cm H2O |
| TD: | 6-8 ml/kg |
| AF: | 5-10 andetag/minut |
| TU: | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP: | 5-10 cm H2O |
| FiO2: | 25-40% |
| CPAP: | 3-7 cm H2O |

PSIMV+
Tryckkontrollerad mode. Om patienten triggar mellan SIMV-andetagen så levereras tryckunderstött andetag.
VK – Volymkontrollerad ventilation
Kontrollerad förutbestämd andning med övertrycksventilation, patienten behöver inte andas själv. Volymen i varje andetag är förutbestämd. Ger alltid ett konstant flöde i inandningsluften. Ger högre topptryck i inandningen (slutinspiratoriskt) jämfört med tryckkontrollerad ventilation. Ger mindre risk för hypoventilation. I volymkontrollerad ventilation är topptrycket högre än platåtrycket. VK används främst vid behandling av lindrig eller måttlig lungsvikt. Vid flöde/volymorienterade andningsmode upprätthålls en konstant inspirationsvolym. Vid dessa andningsmoder kan extra flöde triggas (utlösas) på begäran under inspiration. Ytterligare andetag kan alltså triggas mellan de vanliga andetagen om det inställda triggerkriteriet uppfylls.
- Levererar en förinställd tidalvolym eller minutvolym under en förinställd inspirationstid och vid en förinställd andningsfrekvens, oberoende av förändringar i resistans eller compliance i lungan eller thorax
- Upprätthåller ett konstant flöde med varierande topptryck
VK Volymkontrollerad ventilation - inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| TU: | 5-15 cm H2O |
| TD: | 6-8 ml/kg |
| AF: | 12-20 andetag/minut |
| TU: | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP: | 5-15 cm H2O |
| FiO2: | 25-40% |

TK – Tryckkontrollerad ventilation
Kontrollerad andning, patienten behöver inte andas själv. Ventilatorn ger andetag med ett konstant förinställt tryck med decelererande flöde under en förinställd inspirationstid och med förinställd andetagsfrekvens. Ger alltid ett decelererande flöde i inandningsluften. Ger lägre topptryck jämfört med volymkontrollerad ventilation. Ger mindre risk för tryckskador i lungvävnaden och kan vara av godo vid ARDS. I tryckkontrollerad ventilation är topptrycket lika med platåtrycket. Vid tryckorienterade arbetssätt underhålls en konstant inställd trycknivå under inspiration (tryckkontroll, tryckunderstöd). TK används främst vid behandling av måttlig eller svår lungsvikt.
- Levererar ett konstant tryck under en förinställd inspirationstid och vid en förinställd andningsfrekvens
- Levererar inspiration med ett decelererande flöde
- Förändringar i lungans eller thorax resistans eller compliance påverkar den levererade volymen
TK - inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| TU: | 5-15 cm H2O |
| TD: | 6-8 ml/kg |
| AF: | 12-20 andetag/minut |
| TU: | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP: | 5-15 cm H2O |
| FiO2: | 25-40% |

TU – Tryckunderstödd ventilation
Förutsätter spontanandning och att patienten triggar varje andetag själv. Ventilatorn ger andetag med inställt tryck som är konstant under hela inspirationstiden. Alla andetag är patienttriggade. Ger ett decelererande flöde i inandningsluften. Ger det topptryck som man ställer in. Ger mindre risk för tryckskador i lungvävnaden och kan vara av godo vid ARDS. I tryckunderstödd ventilation är topptrycket lika med platåtrycket. Används främst vid urträning ur respirator och god spontanandning. Vid tryckorienterade arbetssätt underhålls en konstant inställd trycknivå under inspirationen (tryckkontroll, tryckunderstöd). TU används vid behandling av både lindrig, måttlig och svår lungsvikt.
- Initieras av patienten som kontrollerar andningsfrekvens och tidalvolym
- Levererar ventilatorstöd med den förinställda trycknivån och ett avtagande flöde
- Ger backupventilation (TK) i händelse av apné
TU - inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| TU: | 5-15 cm H2O |
| TD: | 6-8 ml/kg |
| AF: | 12-20 andetag/minut |
| TU: | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP: | 5-10 cm H2O |
| FiO2: | 25-40% |
VU – Volymsunderstödd ventilation
- Initieras av patienten som kontrollerar andningsfrekvensen själv
- Levererar ventilatorstöd med ett variabelt topptryck och ett decelererande flöde för att garantera den förinställda tidalvolymen
- Det inspiratoriska trycket i ett andetag kommer aldrig att överskrida 5 cm H20 under den övre tryckgränsen
- Ventilatorn ger backupventilation (VKTS) i händelse av apné
VKTS – Volymkontrollerad tryckstyrning
VKTS innebär kontrollerad andning, patienten behöver inte andas själv. Ger ett decelererande flöde i inandningsluften. Ger ibland högre topptryck jämfört med tryckkontrollerad ventilation. Ger mindre risk för hypoventilation. Styr trycknivån så att tidalvolymen är konstant. Anpassar trycket så att lägsta möjliga tryck ges. VKTS används vid behandling av både lindrig, måttlig och svår lungsvikt.
- VKTS kombinerar fördelarna med volymkontroll och tryckkontroll genom en leverera en förinställd tidalvolym med decelererande inspiratoriskt flöde vid en förinställd andningsfrekvens
- Upprätthåller lägsta möjliga konstanta tryck under hela inspirationen
- Det inspiratoriska trycket i ett andetag kommer aldrig att överskrida 5 cm H2O under den övre tryckgränsen
VKTS - inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| TU: | 5-15 cm H2O |
| TD: | 6-8 ml/kg |
| AF: | 12-20 andetag/minut |
| I:E | 1:2 |
| PEEP: | 5-15 cm H2O |
| FiO2: | 25-40% |

Automode VKTS – VU
- Är en interaktiv mode som automatiskt växlar mellan kontrollerad mode (VK) och understödd mode (VU) baserat på patienttriggning
- Levererar kontrollerade andetag i frånvaro av patientandetagsförsök, men växlar till understödd andning när ett andningsförsök detekteras
- Fungerar som ett hjälpmedel i början av urträningsperioden
- Anpassar sig efter patientens andningskapacitet
Automode VK – VU
- Är en interaktiv mode som automatiskt växlar mellan kontrollerad mode (VK) och understödd mode (VU) baserat på patienttriggning
- Levererar kontrollerade andetag i frånvaro av patientandetagsförsök, men växlar till understödd andning när ett andningsförsök detekteras
- Fungerar som ett hjälpmedel i början av urträningsperioden
- Anpassar sig efter patientens andningskapacitet
Automode TK + TU
- Är en interaktiv mode som automatiskt växlar mellan kontrollerad mode (TK) och understödd mode (TU) baserat på patienttriggning
- Levererar kontrollerade andetag i frånvaro av patientandetagsförsök, men växlar till understödd andning när ett andningsförsök detekteras
- Fungerar som ett hjälpmedel i början av urträningsperioden
- Anpassar sig efter patientens andningskapacitet
NAVA – Neurally Adjusted Ventilatory Assist
- Ventilationen kontrolleras av patienten via Edi, diafragmans elektriska aktivitet
- Ger stöd i proportion till och synkroniserat med patientens andningsförsök
- Kräver att Edi-kateter sätts in för övervakning av Edi i alla lägen och i Stand-by
- Tryckkurvan vid NAVA följer Edis mönster under inspiration
- Det inspiratoriska trycket i ett andetag kommer aldrig att överskrida 5 cm H2O under den övre tryckgränsen Ger backupventilation (PC) vid apné
NAVA styr ventilationen genom att fånga upp de elektriska impulserna i patientens diafragma via en esofaguskateter (Edi). Det finns tre huvudinställningar i NAVA är NAVA-nivå, PEEP och O2-koncentration som alla måste ställas in före start. Det som behövs förutom SERVO-i ventilatorn är mjukvaran för NAVA, en Edi-modul och en Edi-kateter. Edi-katetern läggs ner i esofagus som en vanlig ventrikelsond. NAVA ger god synkroni mellan patient och ventilator och minskar obehaget av ventilatorbehandlingen. NAVA ger möjligheter till lungprotektiv behandling genom att undvika att ge för mycket eller för lite andningsstöd. Optimal synkroni gynnar spontanandningen. Edi signalen kan användas som ett stöd vid beslut angående avvänjning av ventilationsbehandlingen. Edi-signalen kan användas som en övervakningsparameter eftersom den ger information angående ”andningsdriven”, önskad tidalvolym, effekt av ventilatorinställningar och kan ge information angående sedering och urträning ur ventilatorn. Edi-katetern finns tillgänglig i storlekar mellan 6 och 16 Fr. Katetern kan även användas för att ge en esofagusavledning på EKG. Edi signalen erhålls som ett toppvärde och ett dalvärde. När patienten triggar ett andetag flödar gas in med ett variabelt tryck proportionellt mot patientens Edi. Högsta möjliga tryck är 5 cm H2O lägre än förinställd övre tryckgräns. Edi-trigg kan ställas in mellan 0,1 – 2 μV. Ställ in en lägre triggningsnivå om inga andetag ges medan det finns en tillräcklig Edi-signal. Höj Edi-triggningsnivån om det finns en tillräcklig Edi-signal. Höj Edi-triggninigsnivån om för många andetag ges pga brus i signalen. Triggningen visas med en symbol och en färgmarkering på kurvan.
Det finns fyra grundinställningar i NAVA: NAVA nivå, PEEP, O2 konc. och Edi trigg. I ventilatorn ställer man in NAVA level (cmH2O/μV), PEEP (cm H2O), syrgaskoncentration (%) och Trigger Edi (μV). Grundinställning av Trigger Edi är 0.5 μV (0,1 – 2 μV). I pressure support ställer man in trigger sensitivitet, inspiratorisk cykel (off), och tryckunderstöd över PEEP.
NAVA Ppeak = NAVA level x (Edi peak – Edi min) + PEEP. Estimerat NAVA peak visas i respiratordisplayen.
NAVA - inställningar i respiratorn
| Andningsfysiologiska parametrar | Normala inställningar |
|---|---|
| NAVA level | 1,5-2,0 cm H2O/μV |
| Trigger Edi | 0.5 μV |
| PEEP: | 5-10 cm H2O |
| FiO2: | 25-40% |
Respiratorbehandling av barn
- Mindre lungvolym/kg, större anatomiskt dead space, och större andningsarbete än vuxna
- Högre metabolism = högre O2 konsumtion
- En normal expiration i vila gör att lungan hamnar under sin closing capacity
- Avsaknad av bronkioalveolära förbindelser (ökad atelektasrisk)
- Små barn desaturerar snabbt vid apné
- Preoxygenering kan vara svårt vid induktion
- Man har sällan tid att leta efter rätt prylar när det blir allvar…
Ventilation respiratorinställningar
- Vanligtvis tryckkontrollerad ventilation på barn (TK, TU eller VKTS vanligaste mode)
- Tidalvolym vanligen 6-7 ml/kg , PEEP 5 som standard (ibland högre)
- Helst FiO2 < 0,5
- Rekryteringar kan (och bör) göras som vanligt men ger ofta inte lika goda resultat som på vuxna
- Hur mycket läckage som kan tolereras från en okuffad tub är en omdiskuterad fråga…
- NAVA ventilation används ibland (kanske för sällan)
NIV
- Kan köras med hel mask, nasal mask, ”stickpropp” eller nasal tub
- Hel mask fungerar bäst på större barn, nasal mask eller stickpropp på små barn
- Nasal tub kan funka men stör ofta patienterna => mycket fäktande och dålig andning bäst förutsättningar om patienten går från nasal intubation till NIV
- NIV har blivit ovanligt på barn-IVA efter att högflödesgrimmorna kom
- Kräver kompetenta usk för att fungera

Ventilation – tips inför extubation
- Små barn måste vara ganska vakna för att undvika apné efter extubation
- Helst PEEP 5 och TU 5-7, FiO2 < 0,35
- Sug rent i svalg och lediga näsborrar, ge näsdroppar v.b
- Solu Cortef 5 mg/kg (max 100 mg) kan ges när patienten legat i respirator några dagar
- Micronefrin racemiskt adrenalin) i nebulisator är bra för mindre barn som avsvällande i övre luftvägarna, 0,05 ml/kg, max 0,75 ml (ej i tub eller i tät mask)
- Högflödesgrimma är mycket användbart om man tror att det blir jobbigt för patienten efter extubation
Maquet/Siemens (Getinge) ventilatorer
Servo-I Maquet, Siemens Servo 300, Siemens Servo 900 C. Siemens har tagits över av andra företag, Getingekoncernen och Maquet. Servo-I görs av Maquet.
Maquets och Siemens Servoventilatorer använder kontrollerade och understödda andningsmönster
Volymkontrollerad ventilation (VK), Tryckkontrollerad ventilation (TK), Volymkontrollerad tryckstyrning (VKTS), Tryckunderstödd ventilation (TU) och SIMV (Synchronized intermittent mandatory ventilation). Servoventilatorn har Automode, förbättrad volymsupport, nya SIMV kombinationer (synkroniserad intermittent obligatorisk ventilation) samt Open Lung Tool. Siemens Servo 900 C har Volymkontrollerad ventilation (VK) och Tryckkontrollerad ventilation (TK) som bas. Servo-I (Maquet) har volymkontrollerad tryckstyrning (VKTS) som bas men lika goda möjligheter till VK och TK och flera andra andningsmönster. Ventilatorn kan användas för exakta mätningar av kontrollerad, understödd ventilation eller spontanandning/CPAP.
Displayvisning Servo-i
Maquet Siemens (Getinge) ventilatorer - Displayvisning
| Andningsfysiologiska parametrar | Displayvisning | |||
|---|---|---|---|---|
| Luftvägstryck (Paw) | Topptryck | Platåtryck | Medeltryck | PEEP |
| Minutvolym (MV) | Inspiratorisk MV | Utandad MV | Spontan MV | |
| Tidalvolym (VT) | Inandad VT | Utandad VT | ||
| Andningsfrekvens (RR) | RR | Spontan RR | ||
| Andningsarbete (WOB) | WOB hos patient & ventilator | Shallow breathing index (SBI) | ||
| O2-koncentration | Inandad O2- koncentration (FiO2) | |||
| Tidmätning | Inandning-/utandningstid (I:E) | Inandning-/tot. andningstid (TI/TTOT) | Tidskonstant (TC) | |
| Lungmekanik | Andningsmotstånd | Compliance (C) statisk (i respirationssystem) | Dynamisk elastans (E) | |
| Andningstemperatur | 10-40°C | |||
| Kurvformer | Luftvägstryck – tid | Flöde – tid | Volym – tid | CO2 – tid |
| Kapnografi | Endtidal CO2-konc. (etCO2) | Minuteliminering av CO2 | Tidal CO2 eliminering (VTCO2) | |
| Trendvärden | MV, VT, RR, PEEP, R, C, etCO2, topp-, platå- & medeltryck | |||
| Loopar | Paw–V | Flöde–V | ||
| Syrgasmättnad (SpO2) | SpO2 | Puls | ||
Maquet Siemens (Getinge) ventilatorer - normala inställningar i respiratorn
| Andningsfysiologisk parameter | Normala inställningar |
|---|---|
| TU | 5-15 cm H2O |
| TD | 6-8 ml/kg |
| AF | 0-20 andetag/minut |
| TU | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP | 5-15 cm H2O |
| FiO2 | 25-40% |
| ASB | 3-12 cm H2O |
| CPAP | 3-10 cm H2O |

Aisys (ADU)(Datex-Ohmeda – GE Healthcare)
ADU, Aisys Carestation
Aisys har ett flertal olika andningsmode att välja mellan. Volymkontrollerad ventilation (VCV), tryckkontrollerad ventilation (PCV), tryckunderstödd ventilation (PSVPro (Pro=protection)), SIMV (Synchronized intermittent mandatory ventilation, SIMV-VC, SIMV-PC), PCV-VG: tryckkontrollerad ventilation med volymgaranti och CPAP/PSV. Aisys har förbättrad volymsupport och olika nya SIMV kombinationer (synkroniserad intermittent obligatorisk ventilation). Aisys har volymkontrollerad ventilation (VCV) som bas men lika goda möjligheter till TK (PCV-VG) och andra valbara andningsmönster. Ventilatorn kan användas för exakta mätningar av kontrollerad, understödd ventilation eller spontanandning/CPAP-PSV. Ventilatorns tryckluft finns på baksidan av andningssystemet. En precisionsventil kontrollerar gasflödet till patienten. Under inspiration stänger detta gasflöde utandningsventilen och skjuter ned bälgen. Under expiration pressar ett litet flöde utandningsmembranet för att tillföra ett PEEP-tryck.
ADU Aisys Care Station Display
| Andningsfysiologisk parameter | Displayvisning | Man väljer standardskärm alternativt förinställd visning av t ex | Paw-Manom, Loopar, stor kurva eller lokal | |
|---|---|---|---|---|
| Luftvägstryck (Paw) | Topptryck | Platåtryck | Medeltryck | PEEP |
| Minutvolym (MV) | Inspiratorisk MV | Utandad MV | Spontan MV | |
| Tidalvolym (VT) | Inandad VT | Utandad VT | ||
| Andningsfrekvens (RR) | RR | Spontan RR | ||
| Andningsarbete (WOB) | WOB hos patient & ventilator | Shallow breathing index (SBI) | ||
| O2-koncentration | Inandad O2- koncentration (FiO2) | |||
| Tidmätning | Inandning-/utandningstid (I:E) | Inandning-/tot. andningstid (TI/TTOT) | Tidskonstant (TC) | |
| Lungmekanik | Andningsmotstånd | Compliance (C) statisk (i respirationssystem) | Dynamisk elastans (E) | |
| Apnétid | Önskad apnétidsfördröjning | |||
| Andningstemperatur | 10-40°C | |||
| Kurvformer | Luftvägstryck – Tid | Flöde – Tid | Volym – Tid | CO2 – Tid |
| Kapnografi | Endtidal CO2-konc. (etCO2) | Minuteliminering av CO2 | Tidal CO2 eliminering (VTCO2) | |
| Trendvärden | MV, VT, RR, PEEP, R, C, etCO2, topp-, platå- & medeltryck | |||
| Loopar | Paw–V | Flöde–V | ||
| Syrgasmättnad (SpO2) | SpO2 | Puls | ||
ADU Carestation Ventilator
Normala inställningar i respiratorn
| Andningsfysiologisk parameter | Normala inställningar |
|---|---|
| TU | 5-15 cm H2O |
| TD | 6-8 ml/kg |
| AF | 10-20 andetag/minut |
| TU | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP | 5-15 cm H2O |
| FiO2 | 25-40% |
| ASB | 3-12 cm H2O |
| CPAP | 3-10 cm H2O |

Evita XL, Evita 4, Pulmovista (Drägers ventilatorer)
Evita XL, Evita 4, Pulmovista
Drägers ventilatorer använder flera olika andningsmönster (andningsmodus) såsom: IPPV, BiPaP, BiPaP-assist, CPAP + ASB, SIMV, APRV, MMV. Andningsmodus ger olika typer av assisterad eller kontrollerad ventilation via mask eller endotrakealtub. Ventilatorerna har avancerade andningsmode såsom ”the open breathing system” i AutoFlow, APRV samt grafiska stödverktyg integrerade i displayen som standard. Man ställer vanligen in luftvägstrycken i CPAP-andetag samt i assisterade andetag (ASB) med ett normalt tryck på 5-12 cm H2O.
Dräger Evita Ventilator
Displayvisning
| Andningsfysiologisk parameter | Displayvisning | |||
|---|---|---|---|---|
| Luftvägstryck (Paw) | Topptryck | Platåtryck | Medeltryck | PEEP |
| Minutvolym (MV) | Inspiratorisk MV | Spontan MV | MV-läckage | |
| Tidalvolym (VT) | Inandad VT | Utandad VT | Assisterad spontan VT (VTASB) | |
| Andningsfrekvens (RR) | RR | Spontan RR | Obligatorisk RR | |
| Andningsarbete (WOB) | WOB hos patient & ventilator | Shallow breathing index (SBI) | ||
| O2-koncentration | Inandad O2- koncentration (FiO2) | |||
| Tidmätning | Inandning-/utandningstid (I:E) | Inandning-/tot. andningstid (TI/TTOT) | Tidskonstant (TC) | |
| Lungmekanik | Andningsmotstånd | Compliance (C) statisk (i respirationssystem) | Dynamisk elastans (E) | |
| Andningstemperatur | 18-51°C | |||
| Kurvformer | Luftvägstryck – tid | Flöde – tid | Volym – tid | CO2 – tid |
| Kapnografi | Endtidal CO2-konc. (etCO2) | CO2-produktion | CO2-koncentration - tid | ”Dead space” |
| Trendvärden | FiO2, MV, VT, RR, PEEPi R, C, ET-CO2 | |||
| Loopar | Paw–V | Flöde–V | V- CO2 | |
| Syrgasmättnad (SpO2) | SpO2 | Puls | ||
Dräger Evita Ventilator
| Andningsfysiologisk parameter | Normala inställningar |
|---|---|
| TU | 5-15 cm H2O |
| TD | 6-8 ml/kg |
| AF | 10-20 andetag/minut |
| TU | 5-15 cm H2O |
| I:E | 1:2 |
| PEEP | 5-15 cm H2O |
| FiO2 | 25-40% |
| ASB | 3-12 cm H2O |
| CPAP | 3-10 cm H2O |


















