Författare:
Kai Knudsen
Uppdaterad:
5 februari, 2026
Generell anestesi eller med ett enklare ord ”narkos” utgörs av ett tillstånd av inducerad, reversibel och kontrollerad medvetslöshet (”hypnos”) och smärtfrihet (”anestesi”). Generell anestesi kan beskrivas som ett tillstånd där medvetande, minne, nociception och motorisk funktion är temporärt upphävt. Här beskrivs anestesins olika komponenter och dess olika faser.
- Balanserad anestesi
- Inhalationsanestesi – Narkos
- Anestesiinduktion
- PM: Val av induktionsläkemedel vid generell anestesi
- Preoxygenering – syfte, betydelse och metoder
- Rapid Sequence Induction (RSI)
- Underhållsfas av narkos
- Väckning & extubation
- Väckning ur total intravenös anestesi (TIVA) med propofol plus remifentanil och larynxmask
- Uppvakningsfasen
- Pocketguide – Anestesi
- Standardanestesi
- Muskelrelaxantia
- Malign hypertermi
Balanserad anestesi

Generell anestesi eller med ett enklare ord ”narkos” utgörs av ett tillstånd av inducerad, reversibel och kontrollerad medvetslöshet (”hypnos”) och smärtfrihet (”anestesi”) som ofta benämns som ”balanserad anestesi”. Tillståndet kontrolleras och justeras av anestesipersonal med hjälp av flera olika anestesimedel och används för att tillåta kirurgiska eller andra påfrestande invasiva ingrepp under ”sömn och smärtfrihet”. Tidigare var de viktigaste komponenterna som används för balanserad anestesi ett hypnotikum (sömnmedel) för induktion, ett anestesimedel för underhåll av anestesin (inhalationsanestesimedel), ett analgetikum (en stark opioid) och ett muskelrelaxerande medel. Dessa fyra medel är basen i anestesin och hur man använder och styr dessa medel på ett kontrollerat och säkert sätt är själva grunden i balanserad anestesi.
En narkos för kirurgi kan indelas i fyra olika faser; induktion, underhåll, väckning och uppvakning. De tre första faserna sker i regel på en operationsavdelning medan uppvakningsfasen i huvudsak sker på en uppvakningsavdelning, postoperativ avdelning eller intensivvårdsavdelning. Styrningen av en anestesi genom de olika faserna med olika anestesimedel finns beskrivna här i Narkosguiden. Du hittar flera styrkort med olika varianter av anestesimedel för en balanserad anestesi här.
Användningen av anestesimedel har förändrats under senare år men fortfarande gäller att balanserad anestesi går ut på att kunna försätta patienten i ett tillstånd av kontrollerad medvetslöshet där operatören får möjlighet att utföra sitt ingrepp under goda förhållanden samt att bevara patientens olika organfunktioner optimalt med hänsyn till fysiologin. Man kan säga att anestesiologens roll är att upprätthålla ”god homeostas” under kontrollerad medvetslöshet hos patienten.

Med god homeostas menas att trots yttre påverkan upprätthålla en konstant inre miljö som är förenlig med normal funktion hos organismen, vilket inkluderar vitala parametrar såsom puls, blodtryck, temperatur, extracellulärvätskans volym, blodvolym, hjärtminutvolym, makro- och mikrocirkulation, osmolaritet och elektrolytkoncentration, samt koncentrationer av vätejoner (pH), glukos, syrgas, och koldioxid. Vi måste kompensera för blod- och vätskeförluster och upprätthålla normalfysiologiska förhållanden hos patienten så långt det är möjligt. Patienten ska klara av att försättas i ett medvetslöst tillstånd utan rörelser under många timmar på ett onaturligt sätt. Anestesin och graden av medvetslöshet ska vara adekvat och under kontroll under hela ingreppet. Patienten ska aldrig vara för ytligt eller för djupt sövd och tillståndet ska kunna reverseras på ett kontrollerat och säkert sätt.
Den balanserade anestesin styrs genom att balansera fysiologi och farmakologi under yttre påverkan av kirurgi, invasiva ingrepp eller annat trauma. Man arbetar under anestesi främst med cirkulationsfysiologi och respirationsfysiologi men även andra funktioner som immunsystem och hormonella system som påverkas av generell anestesi.
| Negativt inotrop | Vasodilatation | Fyllnadstryck | Hjärtfrekvens | |
|---|---|---|---|---|
| Midazolam | ja | ja | minskar | ökar |
| Propofol | ja | ja | minskar | varierar |
| Fentanyl | nej | ja | minskar | minskar |
| Ketamin | ? | nej | ökar | ökar |
| Isofluran | ja | ja | oförändrat/ökar | ökar |
| Sevofluran | ja | ja | oförändrat/ökar | ökar |
Narkosgasers fysiologiska data
| Lustgas | Isofluran | Desfluran | Sevofluran | |
|---|---|---|---|---|
| MAC1.0 (%) | 104 | 1,2 | 6,6 | 1,8 |
| MAC-awake | ~0,6 MAC | ~0,4 MAC | ~0,4 MAC | ~0,4 MAC |
| Blod λ (fördelningskoefficient) | 0,46 | 1,4 | 0,45 | 0,65 |
| Hjärna λ | 0,49 | 2,2 | 0,55 | 1,1 |
| Fett λ | 1,1 | 70 | 13 | 37 |
| Metabolism (%) | 0 | 0,2 | 0,02 | 5 |
| Luftvägsirritation | 0 | >1,5 MAC | >1 MAC | 0 |
| Leverskada | 0 | <1/106 | <1/107 | 0 |
| Epileptogen aktivitet | 0 | + | 0 | ++ |
För att kunna ge en balanserad anestesi krävs en adekvat övervakning av patientens vakenhet och fysiologi – en god monitorering. Graden av övervakning anpassas efter ingreppets art och tid samt patientens kondition och grundtillstånd. Patienter i god kondition med ASA klass I behöver i regel inte samma övervakning som en patient med ASA klass IV. Ett större och mer omfattande kirurgiskt ingrepp kräver av naturliga skäl mer omfattande monitorering än enkla kirurgiska ingrepp. Äldre och sköra patienter kräver också i regel mer övervakning än unga starka patienter men inte alltid. I regel standardiseras monitoreringen och upplägget efter ingreppet och justeras sedan med hänsyn till den enskilda patienten. Varje specifikt ingrepp har på varje sjukhus ett särskilt ”set-up” som beskrivs i särskilda PM eller lathundar.
Upplägg på operationsbordet
Man måste kunna hantera upplägget av patienten under narkos, dvs skapa goda förutsättningar för kirurgen att arbeta samtidigt som patienten ska kunna överstå ett onaturligt kroppsläge under ibland många timmar utan att få men av det, t ex i form av compartmentsyndrom, trycksår, lungatelektaser, blåstamponad eller neuralgi (känselbortfall). Upplägget av en patient i narkos är ett delat ansvar mellan kirurgsidan och narkossidan. Så långt möjligt görs upplägget medan patienten är vaken men delar görs med patienten sövd. Vissa uppläggningar i speciella ställningar kan endast behållas under en begränsad tid, till exempel Trendelenburg-läge med högläge av benen kan riskera otillräcklig cirkulation i nedre extremiteterna om det kvarstår för länge.
Plexus brachialis är en stor nervfläta som bildas av de nedersta cervikala spinalnerverna och den första thorakala spinalnerven. Plexat passerar mellan nyckelbenet och första revbenet och slutar i axillen med att dela upp sig i 4 stora grenar. Nerverna till armen utgår från plexus radialis. Översträckning av armarna,
liksom sträckning och rotation i nacken kan skada plexus brachialis. Tryck i axillen och mot
hals/axlar får inte förekomma.
Nervus peroneus i underbenet ligger oskyddad och är endast täckt av hud när den svänger runt collum fibulae, på utsidan underbenet strax nedanför knät. Den är därför på detta ställe, mycket känslig för tryck och sträckning. Tänk på detta om patientens ben ”faller ut” mycket och det är en lång operation. Tryck kan ge skada och droppfot och måste förhindras på alla sätt.
Vaddera mellan narkosbåge och överarm vid fixation av armen mot bågen. Kontrollera alltid att det inte är tryck emot patientens arm. Säkerhetsbandet som fixerar patientens ben ska placeras en bit ovanför knät, alltid vadderat.
Patientuppläggning i bukläge där patienten läggs upp innan narkosinduktion


Monitorering
Grunden i övervakningen under anestesi är kontinuerlig mätning av vitalparametrar som puls, blodtryck, EKG och syremättnad. Mätning görs också av muskeltonus vid användning av muskelrelaxerande medel (TOF). Detta utökas vid behov med monitorering av mer invasiv natur som intraarteriellt kontinuerligt blodtryck via artärkateter, centralt ventryck, BIS och annan mätning av central hemodynamik. Delar av övervakningen beskrivs som Non-invasiv monitorering dvs utan penetrerande stick samt Invasiv monitorering, t ex med artärnål och CVK. Mer om monitorering beskrivs på annan plats i Narkosguiden.


Inhalationsanestesi – Narkos
Metoden att söva människor med gas, generell anestesi har en lång tradition och flera olika anestesigaser har använts genom åren. Vanligen används halogenerade derivat av eter (inhalationsanestesimedel) enbart eller i kombination med lustgas för att försätta patienten i en kontrollerad form av medvetslöshet – narkos. Förångade narkosgaser (vaporiserade) såsom isofluran och sevofluran har ett litet terapeutiskt intervall varför överdosering måste undvikas och tillförd mängd gas styras med hög precision via en förgasare. Inhalationsanestesi har fördelen jämfört med intravenösa anestesimedel av att man kontinuerligt kan mäta patientens endtidala koncentrationer/partialtryck i utandningsluften, som i sin tur återspeglar nivåerna i blod och hjärna. Patientens behov av anestesimedel är visserligen åldersberoende men också mycket förutsägbart med små interindividuella variationer.
Anestesigasernas potens uttrycks med hjälp av MAC-konceptet (MAC = minimal alveolar concentration). Begreppet MAC infördes 1965 och uttrycks i procent anestesigas vid 1 atmosfärs tryck (ATM). MAC uttrycker den minsta alveolära koncentration som får hälften av en population (försöksdjur, försökspersoner eller patienter) att inte reagera på definierade stimuli, t ex en hudincision. MAC är ett mått för att jämföra en och samma anestesigas potens mellan olika populationer eller olika anestesigasers effekt på en viss population. Ett annat uttryck för gasernas potens är MAC-awake (0,3-0,5 MAC), den koncentration som krävs för att blockera voluntära reflexer och perceptiv medvetenhet. En fördel med inhalationsanestesi är att man vid en accidentell överdosering lått kan eliminera tillförd gas via patientens utandning vilket ger en god styrbarhet under pågående narkos.
Narkosgasers fysiologiska data
| Lustgas | Isofluran | Desfluran | Sevofluran | |
|---|---|---|---|---|
| MAC1.0 (%) | 104 | 1,2 | 6,6 | 1,8 |
| MAC-awake | ~0,6 MAC | ~0,4 MAC | ~0,4 MAC | ~0,4 MAC |
| Blod λ (fördelningskoefficient) | 0,46 | 1,4 | 0,45 | 0,65 |
| Hjärna λ | 0,49 | 2,2 | 0,55 | 1,1 |
| Fett λ | 1,1 | 70 | 13 | 37 |
| Metabolism (%) | 0 | 0,2 | 0,02 | 5 |
| Luftvägsirritation | 0 | >1,5 MAC | >1 MAC | 0 |
| Leverskada | 0 | <1/106 | <1/107 | 0 |
| Epileptogen aktivitet | 0 | + | 0 | ++ |
Anestesidjupet följs primärt med kliniska parametrar men teknisk utrustning för anestesidjupsmonitorering blir allt bättre och allt vanligare i klinisk praxis. Normalt doserar man anestesigasen efter MAC så att man uppnår ett MAC på 0,6-1,0 om man samtidigt ger remifentanil i kontinuerlig infusion. Ger man i stället fentanyl i tillägg till gas men använder gas i första hand lägger man sig normalt på ett MAC mellan 0,8 och 1,4. Förgasaren för narkosmedlet doseras i procent, men effekten avläses i MAC. Vid ungefär 2 MAC upphör spontanandning och vid 3 MAC fallerar hjärtat och cirkulationen kollapsar. Samtidig användning av lustgas minskar behovet av vaporiserad gas och ökar därför säkerhetsmarginalen. Grovt sätt är effekten av två kombinerade gaser additiv. Användningen av lustgas har dock av flera olika skäl minskat betydligt under senare år och används numera mest vid induktion av inhalationsanestesi på barn och i samband med förlossningsanalgesi. Vid långvariga narkoser ger ett konstant MAC en successivt högre koncentration i hjärnan varför MAC bör justeras ner något med tiden. Behovet av opioider och muskelrelaxantia är kraftigt reducerat under inhalationsanestesi vilket kan vara en fördel.

Inhalationsanestesi kan indelas i narkoser med kontrollerad andning och narkoser med bibehållen spontanandning. Spontanandningsnarkoser, då givetvis muskelrelaxantia inte används alls, är möjliga vid användning av gaser via andningsmask, larynxmask eller endotrakeal intubation. Eftersom tryckgradienten över en larynxmask är lägre och därmed risken för gasläckage mindre jämfört med masknarkos, krävs mindre ofta intubation. Spontanandning är inte bara fysiologiskt, det ger dessutom på köpet ett korrekt narkosdjup jämfört med kontrollerad övertrycksventilation. I annat fall än korrekt narkosdjup, d.v.s. vid för djup eller för ytlig narkos fungerar det helt enkelt inte och det syns och märks på patienten. Hur man noterar för djup eller för ytlig narkos är lite av ett konsthantverk och kräver en del rutin av narkotisören. Oro hos patienten kan bero på både för ytlig och för djup narkos. En otillfredsställande luftväg ger aldrig bra möjligheter till en god narkos och adekvat narkosdjup. Fri luftväg är sålunda A och O vid spontanandningsnarkos vilket ibland kan vara besvärligt både vid masknarkoser och larynxmasknarkoser. Luftvägen är inte ens garanterat fri när patienten är intuberad. Anestesidjupsmonitorering kan hjälpa men är inte alltid tillförlitligt.

Eftersom narkosgaskoncentrationen är mätbar och narkosdjupet förutsägbart, har man inte alltid behov av annan anestesidjupsmonitorering såsom BIS eller ”Entropy” vid spontanandningsnarkoser. Anestesidjupsmonitorering kan dock vara ett bra hjälpmedel för att undvika för djup anestesi och för långsam väckning.
Tiden för uppvakning är beroende av gasens/gasernas vävnadslöslighet och tillförd mängd inhalationsanestesimedel. Desfluran har ungefär halva sevofluranets löslighet, som i sin tur är hälften så lösligt som isofluran. Lustgasen är väsentligt mindre löslig, i synnerhet i fett jämfört med vaporiserade gaser. Moderna narkosgaser ger ett snabbt och förutsägbart uppvaknande, jämför ”MAC awake”.
Under 90-talet gjordes stora ansträngningar att införa dagkirurgi i klinisk praxis. Detta främst för kostnadseffektivisering och snabbare hemgång. Det blev då intressant med kortverkande narkosmedel i avsikt att snabbt kunna väcka och skicka hem patienter efter kirurgi. Tidigare hade sevofluran och desfluran ansetts olämpliga pga. en hög metaboliseringsgrad med fluoridbildning respektive kokpunkt vid rumstemperatur. Läkemedelsindustrin satsade stora resurser på dokumentation och marknadsföring av dessa båda gaser. Detta bidrog till en ökad kunskap om och intresse för inhalationsanestesi i allmänhet.
Under decenniers användning har man funnit att lustgas kan ge expansion av gasfyllda hålrum, hämning av B-vitaminmetabolismen (kliniskt relevant främst vid sövning av veganer och vid vissa ovanliga genetiska ”inborn errors of metabolism”), en lätt ökning av frekvensen postoperativt illamående, samt diffusionshypoxi (som förutsätter hypoventilation och/eller luftandning utan syrgastillskott). Även förmodat negativa effekter i närmiljö och växthuseffekter i atmosfären gjorde att man önskade eliminera lustgasen från sjukhusmiljön. Eftersom lustgas i kombination med annan vaporiserad gas utgör ungefär halva narkosdjupet, så skulle ett avskaffande av lustgas innebära en betydligt högre förbrukning av sevofluran och desfluran.
Idag används i Sverige huvudsakligen sevofluran i klinisk praxis men även desfluran har fått stor spridning. Den vid introduktionen befarade risken för njurskador av sevofluran har lyckligtvis inte infriats. Såväl ”compound A” från cirkelsystemets koldioxidabsorber som flourider vid metaboliseringen skulle ju teoretiskt kunna vara nefrotoxiska. Ironiskt nog ger emellertid den gamla kombinationen isofluran/lustgas ett snabbare uppvaknande än en ren sevoflurannarkos. Det påstått snabba uppvaknandet var ju den huvudsakliga poängen vid sevoflurans lansering. En fördel, inte minst vid barnnarkoser, är dock att gasinduktion är lättare att genomföra med sevofluran. Patenttiden för sevofluran och desfluran har gått ut och inhalationsanestesi är inte längre ett hett debattämne varför alternativa men inte nödvändigtvis för patienten bättre anestesimetoder vunnit terräng.
Anestesiinduktion

Induktion – narkosinledning
Induktion, dvs uppstart av en narkos innebär att man försätter patienten i sömn, eller mer korrekt i ett kontrollerat stadium av medvetslöshet (anestesi). Intravenös induktion är standard för de flesta anestesiologiska procedurer. Vägen dit går genom förändrad vakenhet i olika stadier, olika narkosdjup i olika hastighet beroende på vilken teknik som används. Efter tillförsel av anestesimedel går man i regel igenom ett kort stadium av relaxation och desinhibition, därefter ett kort stadium av excitation och därefter in i det stadium som ofta benämns kirurgisk anestesi med relaxation av muskeltonus och nedsatt eller upphörd andning.

Under induktionen påverkas andning, vakenhet, ögonens rörelser och koordination samt pupillernas storlek, reflexer, muskeltonus och andra väsentliga fysiologiska funktioner. Det är angeläget att försöka gå genom induktionsstadiet så smidigt som möjligt utan uttalad påverkan på puls och blodtryck. Man bör försöka undvika uttalat blodtrycksfall men ett lindrigt blodtrycksfall är vanligt och de flesta patienter som inte är påtagligt hjärt- och kärlsjuka tolererar detta väl. Vid induktion av sköra patienter är det lämpligt att samtidigt ge ett blodtryckshöjande medel för att undvika anestesimedlens blodtrycksdämpande effekter.
Induktionen startar i regel med preoxygenering med syrgas via mask med patienten i ”sniffing position” för att förbereda övertag av patientens andning och nedläggning av en larynxmask eller endotrakeal intubation. När patienten är väl syresatt inleder man antingen genom intravenös injektion av anestesimedel eller genom inhalation på mask av ett inhalationsanestetiskt medel, en ”narkosgas”. Intravenös induktion är i regel snabbare, mer kontrollerad och mer förutsägbar än inledning på mask via inhalation.
Induktion av anestesi med intravenösa induktionsmedel
PM: Val av induktionsläkemedel vid generell anestesi
Syfte
Att stödja val av intravenöst induktionsläkemedel baserat på patientens fysiologi, kliniska situation och riskprofil för att optimera patientsäkerhet vid anestesiinduktion.
Indikationsstyrt val av induktionsmedel
1. Hemodynamiskt instabil patient
(chock, svår hjärtsvikt, kardiomyopati)
- Förstahandsval: Ketamin vid hypotension eller bronkospasm
- Alternativ: Etomidat
- Obs: Vid uttalad katekolaminbrist kan ketamins blodtryckshöjande effekt utebli
2. Reaktiva luftvägar / bronkospasm
(astma, KOL-exacerbation)
- Förstahandsval: Ketamin
- Alternativ: Propofol
- Obs: Risk för hypotension och apné
3. Neurokirurgiska patienter / misstänkt förhöjt intrakraniellt tryck
- Rekommenderat: Propofol (eller Etomidat)
- Kommentar:
- Båda minskar cerebral metabolism och intrakraniellt tryck
- Ketamin kan övervägas vid kontrollerad ventilation (IVA), praxis varierar
4. Hög aspirationsrisk / Rapid Sequence Induction (RSI)
- Val styrs av hemodynamisk status:
- Stabil patient: Propofol
- Instabil patient: (Etomidat)
- Hypotension / astma: Ketamin
- Muskelrelaxantia väljs separat (t.ex. suxameton eller rokuronium)
5. Behov av samtidig analgesi vid induktion
- Val: Ketamin
- Enda induktionsmedlet i denna grupp med uttalad analgetisk effekt
Sammanfattande minnesregler
- Propofol: Mjuk induktion, antiemetisk – risk för hypotension
- Etomidat: Cirkulatoriskt stabilt – risk för binjurehämning och myoklonier
- Ketamin: Höjer BT, bronkdilaterar, ger analgesi – risk för emergence och hypersalivation
- Tiopental: Snabb effekt – porfyririsk, ackumulation
- Midazolam: Amnesi – olämpligt som ensamt induktionsmedel
Propofol
- Koncentration: 5 mg/ml, 10 mg/ml, 20 mg/ml
- Induktionsdos för anestesi: 2 mg/kg (barn – 2,5-3,5 mg/kg)
- Sedationsbolus: 0,5 mg/kg
- Underhållsanestesi: 4-10 mg/kg/h i minskande dos, TCI 2-6 ug/ml, Sedation: 0,5-4 mg/kg/h
- Undvik: Anestesi med TCI till barn < 16 år

Tiopental (Pentocur)
- Koncentration: 25 mg/ml
- Induktionsdos för anestesi: 4-6 mg/kg (70 kg -14 ml)
- Försiktighet: porfyri, övre luftvägsobstruktion, astmaattacker, extravasal och intrarteriell injektion
Ketamin (Ketalar)
- Koncentration: 10 mg/ml iv, 50 mg/ml im
- Induktionsdos för anestesi: 1-2 mg/kg iv, (5)-10 mg/kg im + midazolam 1-3 mg (tyst på golvet)
- Underhållsanestesi: 0,5-4 mg/kg/h iv i minskande dos
- Smärtlindring efter operation: 5-15 mg i bolus
- Underhållsinfusion: 0,05-0,5 mg/kg/h
- Försiktighet: Högt blodtryck (relativ kontraindikation). Vid leversvikt -> dosreduktion
Esketamin (Ketanest)
- Koncentration: 5 mg/ml iv, 25 mg/ml im => använd halva ketamindosen
Induktion på mask (”Maskanestesi”)
Inhalation via inandning av narkosgas på mask används mest på barn där man vill vänta med att lägga in en intravenös infart (venkanyl) tills barnet somnat och inte upplever smärta. Detta kräver god kännedom om narkosgasers effekter och god förmåga att hantera luftvägen när barnet somnar in och går igenom de olika faserna av anestesiinledningen. Under inledning på mask blir excitationsfasen kraftigare och mer utdragen än vid intravenös inledning. I regel börjar man med spontanandning för att gradvis gå över till manuellt kontrollerad andning samtidigt som narkosdjupet fördjupas med inhalationsanestesimedel via förgasare. Man bör vara varsam men stadig på handen då kraftiga manipulationer av luftvägen under excitationsfasen kan trigga en laryngospasm som kan försvåra anestesiinledningen och skapa svårigheter att fördjupa anestesidjupet till rätt nivå. Nedförandet av en svalgtub kan förbättra luftvägen och möjliggöra manuell ventilation så att excitationsstadiet passeras på rätt sätt samtidigt som det kan trigga en laryngospasm om det görs när patienten är för ytligt sövd. Anestesigasen måste tillföras i rätt takt då allt för snabb tillförsel kan ge apné eller laryngospasm eller trigga orolig patient. Ofrivilliga okontrollerade rörelser under denna fas är vanligt. En kraftig excitation kan orsaka kraftigt stresspåslag med takykardi och blodtrycksstegring följt av ett kraftigt och farligt blodtrycksfall när excitationen passeras och bör därför undvikas.

Inledning på mask av vuxna patienter görs numera sällan men var vanligare förr. Det kan göras i undantagsfall, t.ex. av patient med uttalad stickrädsla eller patient med grav autism. Det är dock undertecknads personliga erfarenhet att patienter som är så pass uttalat stickrädd att man vägrar intravenös inledning också kan erbjuda svårigheter med inledning via inhalation. Bäst väg att komma till rätta med detta problem är i regel genom god preoperativ information och en stark premedicinering samt effektiv topisk anestesi för att kunna sätta nål i en ven. Annan anledning kan vara extremt svårstucken patient som har fått nog av multipla stickförsök i vaket tillstånd.

Intravenös induktion
Intravenös induktion med snabbverkande anestesimedel är standard vid de flesta anestesier, såväl till barn som till vuxna. Anestesin förbereds med en god premedicinering, vid behov topisk anestesi (hudbedövning) samt inläggande av en venkanyl i en perifer ven (”sätta nål”). Efter standardiserade förberedelser på sal och check-in startar anestesin med injektioner av snabbverkande insomningsmedel som antingen ges manuellt i en perifer venkanyl eller via infusionspump eller i kombination av manuella injektioner och injektion via injektionspump (sprutpump). I en traditionell narkos ges medlen för hand via injektioner med spruta. Vanligt är att man inleder med en stark opioid som fentanyl eller alfentanil under cirka två minuter. Härefter avvaktar man tills man noterar att patienten reagerar adekvat på given dos vilket också verifierar att den venösa infarten fungerar som den ska. I nästa steg ger man en dos av ett hypnotikum, vanligen propofol men även andra medel kan användas som pentothal, ketamin eller etomidat. Dosen justeras efter ålder, vikt, kondition och aktuellt tillstånd.


I vanlig induktion ges muskelrelaxerande medel i form av icke depolariserande medel när patienten ”sover gott” efter inledningen dvs inte reagerar med blinkreflex eller vid beröring ca 1-2 minuter efter att hypnotika givits. Efter att muskelrelaxerande medel givits startar man i regel en ”timer” och ger patienten kontrollerade andetag genom manuell övertrycksventilation via andningsmask och blåsa. Denna manuella ventilation pågår i 90-120 sekunder varefter intubation eller nedläggning av larynxmask kan genomföras. Efter säkerställd luftväg kontrolleras denna genom auskultation med stetoskop samt kontroll av utandningsluften med endtidalt uppmätt koldioxidvariation.
Härefter kopplas vanligen en anestesigas in, till exempel sevofluran eller desfluran och anestesin övergår i nästa fas, underhållsfasen. Användandet av muskelrelaxerande medel styrs efter huruvida det hjälper kirurgen dvs om det är nödvändigt för att kunna penetrera buken eller att patienten behöver ligga helt still. Muskelrelaxerande medel kan också vara nödvändigt för att kunna ventilera patienten på bästa sätt och koordinera med kirurgin, till exempel vid thoracoabdominella ingrepp.
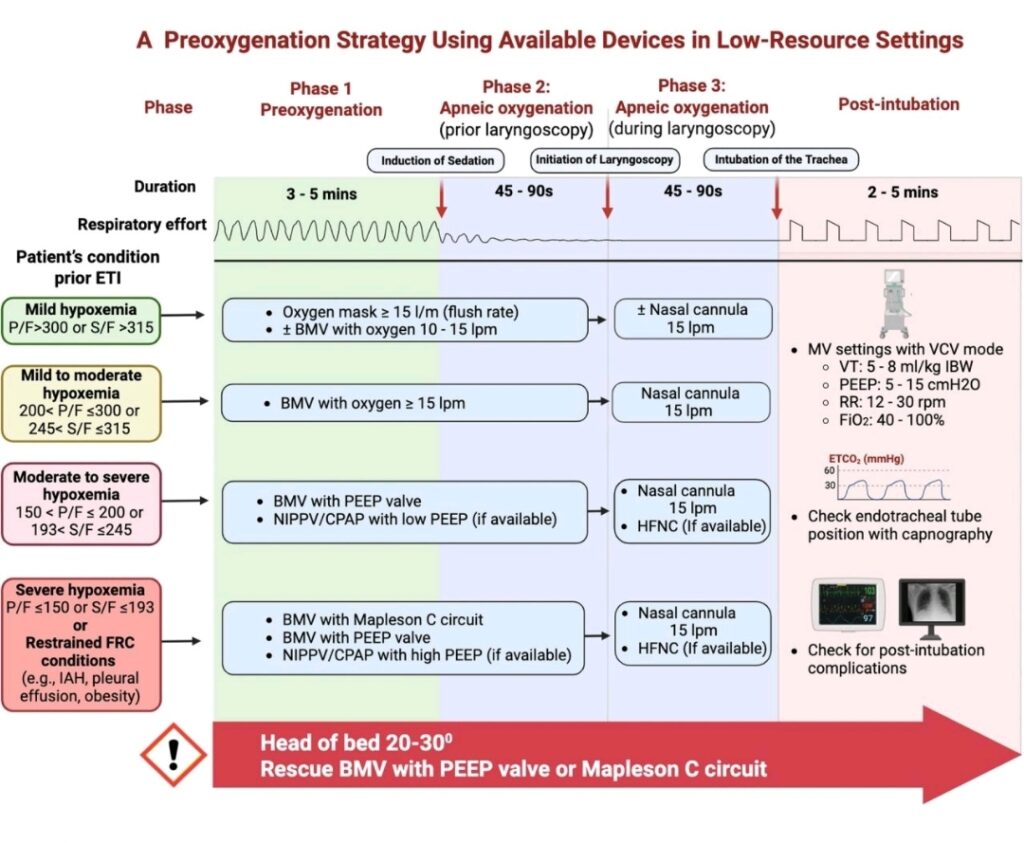
Preoxygenering – syfte, betydelse och metoder
Preoxygenering är en grundläggande anestesiologisk åtgärd som syftar till att maximera säker apnétid inför induktion av anestesi. Genom att ersätta kvävet i lungorna med syrgas ökas kroppens syrgasreserv, vilket förlänger den tid patienten kan tolerera apné innan hemoglobinsyremättnaden sjunker till kritiska nivåer. Detta förbättrar säkerhetsmarginalen vid luftvägshantering och intubation.
Varför preoxygenering är nödvändig
Vid induktion av anestesi finns en betydande risk för snabb utveckling av hypoxemi. Detta beror bland annat på hypoventilation eller apné, minskad funktionell residualkapacitet (FRC) till följd av ryggläge, muskelrelaxation och anestetiska läkemedel. Risken är särskilt uttalad vid svår maskventilation, svår intubation samt hos patienter med obesitas, gravida och barn. Därför rekommenderas rutinmässig preoxygenering före generell anestesi.
Säker apnétid
Den säkra apnétiden (tiden till SpO₂ sjunker till cirka 80 %) varierar mellan patientgrupper.
Hos friska, normalviktiga vuxna kan den uppgå till cirka 9 minuter, medan den hos barn och överviktiga vuxna ofta är 3 minuter eller kortare, vilket understryker vikten av effektiv preoxygenering i dessa grupper.
Teknik för adekvat preoxygenering
Preoxygenering utförs med 100 % syrgas via tättslutande ansiktsmask, kopplad till anestesiapparat eller Mapleson-system. Rekommenderat flöde är 10–12 liter per minut, tillräckligt för att förhindra återandning. Det är avgörande att masken sluter tätt och att end-tidal syrgaskoncentration (EtO₂) överstiger 90 %, vilket indikerar optimal preoxygenering och maximal apnétid.
Metoder för preoxygenering
- Tidalvolymsventilation (gold standard)
Patienten andas normalt via ansiktsmask i cirka 3 minuter. Denna metod ersätter upp till 95 % av lungornas gasinnehåll och är den mest effektiva. - Vital capacity breaths (snabb metod)
Alternativ vid tidsbrist, exempelvis vid snabb induktion. Fyra djupa andetag under 30 sekunder är mindre effektivt, medan åtta andetag under 60 sekunder ger bättre effekt och kan vara acceptabelt i vissa situationer. - THRIVE (Transnasal Humidified Rapid-Insufflation Ventilatory Exchange)
Högflödesnasal syrgas (cirka 60 L/min) under 3 minuter. Metoden kan vara lika effektiv som traditionell preoxygenering med ansiktsmask och har fördelen att kunna fortsätta under apné.
Mål
Målet med preoxygenering är att uppnå end-tidal O₂ >90 % före anestesiinduktion, vilket ger maximal syrgasreserv och ökad patientsäkerhet vid luftvägshantering.
Rapid Sequence Induction (RSI)
Vid sövning av patient med ökad risk för luftvägsaspiration av magsäcksinnehåll sövs patienten med en så kallad RSI-teknik: ”Rapid Sequence Induction”. Med denna teknik placeras huvudändan i förhöjt läge, så kallad ”sniffing position”. Patienten preoxygeneras noggrant via spontanandning på tättslutande mask med 100% syrgas varefter induktionsmedlen ges i snabb följd med analgetika, hypnotika och muskelrelaxerande medel. Direkt efter intuberas patienten utan kontrollerad övertrycksventilation. Man kan samtidigt använda cricoid-tryck men detta har ifrågasatts under senare år då det kan försvåra intubationen och nyttan är tveksam. Exempel på fall med ökad risk för aspiration är tarmparalys (ileus) och akuta patienter som inte fastat tillräckligt länge.
”Snabb sekvensintubation”
1. Förbered rätt utrustning
- Intravenös infart
- EKG
- SpO₂-övervakning
- Rubens blåsa (BVM) med PEEP
- Sug
- Endotrakealtub (ETT) + ledare (stylet)
- ETCO₂-kurva (kapnometri)
- Alternativ luftväg (LMA / i-gel)
- Utrustning för krikotyrotomi
Immobilisera halsryggen vid trauma
2. Preoxygenering
- 100 % O₂ i 3 minuter eller 8 andetag med vital kapacitet
- Non-rebreather-mask + näsgrimma 15 L/min (apné-syrgas)
- Vid hypoxi → ventilera med BVM + PEEP
Krikoidtryck:
Rekommenderas inte rutinmässigt (ingen bevisad nytta, kan försämra sikten).
Använd endast om lokala riktlinjer fortfarande kräver det.
3. Induktionsläkemedel – välj ett alternativ
- Ketamin 1–2 mg/kg i.v.
- Bra vid hypotension, astma, status asthmaticus
- Ökar blodtryck och hjärtfrekvens (fördel vid chock)
- Propofol 1–2 mg/kg i.v. (snabbt anslag)
- Bra vid skallskada (↓ ICP)
- Undvik vid hypotension
- Midazolam 0,1–0,3 mg/kg i.v. (långsammare anslag)
- Tiopental 1–3 mg/kg i.v. (används sällan idag)
- Diazepam 0,2 mg/kg (ej förstahandsval)
4. Förbehandling – välj ett alternativ
- Atropin 0,02 mg/kg i.v.
- Spädbarn <1 år, eller vid användning av succinylkolin
- Förebygger reflexutlöst bradykardi
- Lidokain (föråldrat)
- Tidigare använt vid förhöjt ICP, rekommenderas ej rutinmässigt
5. Muskelrelaxantia
- Succinylkolin 1–1,5 mg/kg i.v.
- Snabbast anslag (45–60 sek)
- Undvik vid:
- Brännskador >24 timmar
- Klämskador
- Stroke >48 timmar
- Neuromuskulära sjukdomar
- Hyperkalemi
- Risk för malign hypertermi
- Rokuronium 1,2 mg/kg i.v. (modern RSI-dos)
- Snabbt anslag (60–90 sek)
- Bra alternativ till succinylkolin
- Lång duration (45–60 min)
- Vekuronium 0,1 mg/kg i.v.
- Långsammare anslag, ej optimalt för RSI
6. Intubation
- Sniffing-position eller ”ramped position”
- Använd videolaryngoskop om tillgängligt (numera standard)
- För in bladet, för tungan åt vänster, lyft ordentligt
- Visualisera glottis
- För tuben genom stämbanden
7. Bekräfta tubens läge
- Kontinuerlig endtidal kapnografi (ETCO₂) = standard
- Bilateral bröstkorgshöjning
- Bilaterala andningsljud
- Inga ventrikelljud
- Imma i tuben
- Stabil och förbättrande SpO₂
- Tubdjup: 3 × ETT-storlek
- Exempel: 7,0-tub → 21 cm
8. Säkra tuben & fortsatt vård efter intubation
- Blås upp kuffen
- Fixera tuben med hållare eller tejp
- Ställ in respiratorn
- Sedationsinfusion (propofol, midazolam, ketamin)
- Analgesi (fentanyl)
- Kontinuerlig övervakning
- Omvärdera efter varje patientförflyttning
Underhållsfas av narkos
Under underhållsfasen styrs anestesin efter principen om god homeostas där narkosen anpassas efter ingreppets art och omfattning. En god kontinuerlig kommunikation mellan narkosen och kirurgen är nödvändigt för att detta ska fungera väl. Detta är den fas där kirurgin utförs. Man kontrollerar och anpassar anestesin efter puls, blodtryck, temperatur, syremättnad, extracellulärvätskans volym, blodvolym och hjärtminutvolym. Vakenheten eller graden av medvetslöshet monitoreras kliniskt eller med hjälp av anestesidjupsmätare som BIS eller Entropy, ett värde mellan 40 och 60% eftersträvas normalt och man försöker undvika för ytlig eller för djup sömn.

Anestesin underhålls med antingen intermittenta doser av intravenösa medel som fentanyl i kombination med ett inhalationsanestesimedel som sevofluran, eller med en kontinuerlig infusion av en opioid i kombination med ett inhalationsanestesimedel eller enbart med intravenösa medel, t ex propofol och remifentanil. Använder man enbart intravenösa medel kallas anestesimetoden för Total Intravenös Anestesi (TIVA) medan den kombinerade tekniken med inhalationsanestesimedel kallas för Balanserad anestesi. Vilken teknik som föredras kan styras av anestesiologen och har ofta sin grund i ingreppets art samt lokala rutiner och praxis. Somliga föredrar en inhalationsstyrd teknik medan andra föredrar den intravenösa tekniken och åter andra föredrar den kombinerade tekniken. Båda tekniker är väl beprövade och väl fungerande. Graden av tillförsel av anestesimedel styrs efter kirurgin samt efter patientens vakenhet och fysiologiska tillstånd. Anestesi är alltid ett dynamiskt tillstånd med kontinuerliga variationer som gör det till ett spännande och utmanande arbete. Förändringar i fysiologin och inställningar i anestesin journalförs kontinuerligt i den s.k. narkoskurvan. Narkoskurvan har i alla år varit en pappersjournal som skrivs kontinuerligt av narkossköterskan under hela ingreppet från start till avslut men under senare år har mer och mer information digitaliserats och vissa kliniker använder enbart digitala system. När operationen eller interventionen under narkos närmar sig slutet anpassas anestesin efter detta, anestesimedlen nedregleras och man går in i nästa fas, väckningsfasen.

Vasopressorstöd mot blodtrycksfall
Efedrin
- Indikation: Blodtrycksfall, bronkialastma
- Koncentration: 5 mg/ml
- Direkt receptagonist + NA-frisätt –> α1 +, β1+++, β2 ++ = SVR↑, CO↑, HR↑, BT↑
- Dosering: 5-10 mg iv -effekt 10-15 min (för mer långvarig effekt kan 25-50 mg ges im el sc)
- Biverkningar: Takykardi, arytmier, coronarischemi
Fenylefrin
- Dosering: 0,1-0,2 mg iv, alt infusion 0,05-0,15 μg/kg/min iv = cirka 3 – 20 ml/h för 70 kg
- Koncentration: 0,1 mg/ml
- Fysiologiska effekter: α1 ++++ = SVR↑, CO↓, HR↓, BT↑
- Biverkningar: Bradykardi, hjärtsvikt, lungödem
Noradrenalin
- Indikation: Sepsis, anafylaktisk chock, hypotension med SVR↓↓
- Fysiologiska effekter: α1 ++++, β1+++, β2+ (SVR↑, CO±0, HR↑, BT↑↑
- Dosering: 0,01-0,5 μg/kg/min = 0,5-40 ml/h för 70 kg (0,1 mg/ml)
Väckning & extubation
Mot slutet av det kirurgiska ingreppet anpassas anestesin efter att patienten ska väckas ur narkosen. Anestesimedlen skruvas ner så att effekten avtar och patienten stiger i vakenhet. Detta anpassas efter kirurgin, patienten ska i regel vara väl sövd tills sista stygnet är satt, alternativt tills patienten är vänd i rätt position för väckning, t ex från bukläge till ryggläge. Operationssåret ska förslutas och förband ska läggas före väckning. All steril operationsklädsel ska tas bort i en ”avdukning” och en ”avtäckning” vilket i regel går relativt fort. Infarter, ev. sårdrän och dropp ska justeras och anpassas till den postoperativa fasen. Patienter utan blåskateter ska i regel genomgå en s.k ”Bladder scanning” där volymen urin i blåsan mäts och ev. tappas ut innan väckning ur anestesin. Patienten ska sedan extuberas eller larynxmasken tas bort och det sker när patienten vaknar upp och kan klara sin egen spontanandning på ett betryggande sätt.

Själva väckningen går i regel till genom att anestesimedlen stängs av och patienten vaknar av sig självt när de sövande effekterna klingar av. Avstängningen av anestesimedel och utvädring av anestesigaser anpassas efter operationsavslutet. Patienten vaknar i regel när spontanandningen är stabil och MAC värdet på gasen är nere på 0.1%. Alternativt kan vissa antidoter ges, t ex naloxon för att bryta opioideffekten men antidoter används restriktivt för att undvika smärtgenombrott. I stället ges vanligen något mer långverkande analgetikum, t ex morfin mot slutet av operationen för att patienten ska vara smärtfri när hen vaknar ur narkosen. Patienter som varit sövda med enbart intravenös teknik vaknar i regel till snabbare och bättre jämfört med patienter som fått inhalationsanestesimedel. Reversering av de muskelrelaxerande effekterna görs rutinmässigt mot slutet av anestesin efter klinisk bedömning eller efter mätning av muskelaktiviteten genom TOF-mätning, v.g. se särskilt kapitel i Narkosguiden om muskelrelaxerande medel. Vanligen reverseras muskelrelaxantia genom att ett cholinesterashämmande medel som neostigmin ges i kombination med ett antikolinergikum (Atropin/Neostigmin). Alternativt kan antidoten sugamadex användas. Patienten extuberas inte förrän man har förvissat sig om att adekvat muskelstyrka återkommit och muskelrelaxationen reverserats, t ex att patienten kan krama handen med fast grepp eller lyfta huvudet från kudden och framför allt bibehålla god andning. Otillräcklig muskelaktivitet kan se ut som ytlig kippande andning vilket har beskrivits ”som en fisk på torra land” vilket är ett potentiellt livshotande tillstånd.
När patienten vaknar upp extuberas vederbörande, dvs endotrakealtub eller larynxmask tas bort och svalget rensugs från slem. Detta görs kontrollerat när patienten kan andas tillfredställande och kan titta upp och ge ögonkontakt. Är patienten orolig med oregelbunden andning, kan inte ge ögonkontakt eller har påtaglig luftvägsirritation (apné) kan det löna sig att ge en liten dos propofol 20-40 mg för att relaxera patienten och kunna eliminera mer av anestesigaser som förbättrar förhållandena för extubation. Respiratoriskt bör patienten kunna klara av sin andning med högst 5 cm PEEP och 35% syrgas för att kunna extuberas säkert. Efter extubationen ska patienten kunna klara sig med egen spontanandning och bibehålla fri luftväg även i ryggläge. Vanligtvis ges syrgas på grimma eller andningsmask under uppvakningsfasen.
Kriterier för extubation
- Spontan ögonöppning
- Ansiktsgrimas
- Patientrörelse annan än hosta
- Konjugerad blick
- Målmedvetna rörelser
- Endtidala nivåer av anestesigas lägre än:
- Sevofluran: 0,2%
- Isofluran: 0,15%
- Desfluran: 1,0%
- Syremättnad högre än 97%
- Positivt larynxstimuleringstest
- Endtidal volym större än 5 ml/kg
Efter kirurgi på väldigt sköra patienter eller efter större ingrepp eller vid respiratoriska problem bibehålls inte sällan endotrakealtuben och patienten går in sederad till intensivvården eller den postoperativa vården fortsatt kopplad till en ventilator för en senare extubation i mer stabilt läge. Är man osäker på om patienten kan klara en extubation är det bättre att bibehålla tuben till ett senare skede, t ex om patienten blivit hypoterm, är cirkulatoriskt instabil eller vid stor eller pågående blödning. Förflyttningen av patienten sker då i regel med en s.k. transportventilator in till postop eller IVA.
Väckning ur total intravenös anestesi (TIVA) med propofol plus remifentanil och larynxmask
Väckning ur anestesin ska ske kontrollerat och i nära samarbete mellan anestesipersonal och operatör för att säkerställa adekvat analgesi, stabil andning och säker luftväg.
Inför suturering ska operatören uppmanas att lägga lokalbedövning för att minska nociceptiv stimulering under den avslutande fasen av anestesin. En 10 ml spruta med propofol ska vara uppdragen och tillgänglig som backup vid behov av snabb fördjupning av anestesin.
När subkutana stygn påbörjas sänks propofolinfusionen till 2,0 CPT samtidigt som remifentanil justeras till 2,0. När hudsuturen inleds reduceras propofol ytterligare till 1,5 CPT medan remifentanil bibehålls på 2,0. När cirka 3–4 hudstygn återstår pausas båda infusionerna. Pumparna ska inte stängas av, utan endast pausas, för att möjliggöra snabb återstart vid behov.
Narkosläkare ska tillkallas i samband med väckningsfasen enligt lokal rutin eller vid minsta osäkerhet kring patientens tillstånd. Larynxmasken tas ur svalget när patienten vaknar upp och kan gapa voluntärt.
Om patienten inte har vaknat vid avdrapering ska patienten flyttas över till säng med larynxmask (LMA) kvar på plats och fortsatt övervakning ske tills adekvat spontanandning och skyddsreflexer föreligger. Larynxmasken kan då tas bort när patienten ligger i sängen
Under hela väckningsförloppet ska särskild uppmärksamhet riktas mot andning, cirkulation, syresättning och medvetandegrad för att säkerställa en trygg och kontrollerad övergång till postoperativ fas.
Uppvakningsfasen
När patienten är väckt ur narkosen och operationen avslutad ska patienten under stabila förhållanden flyttas över till en uppvakningsavdelning eller en postoperativ avdelning (”Postop”). I regel sker väckningen på operationssalen på operationsbordet och patienten flyttas därefter över i sin säng men vid vissa tillfällen flyttas patienten först över i sängen och väcks sedan där. Detta sker t ex när förflyttningen kan förväntas bli smärtsam eller när det är viktigt att undvika okontrollerade rörelser. Omvänt inleds vissa narkoser i sängen i stället för på operationsbordet när förflyttningen förväntas bli smärtsam, t ex vid akuta frakturer.
Uppvakningen sköts i regel av annan personal än narkospersonal på en postoperativ avdelning. Tiden på postop avgörs av ingreppets art och patientens tillstånd. Stor kirurgi kräver av naturliga skäl längre tid på postop men detta varierar från fall till fall. På den postoperativa avdelningen är det viktigt med fortsatt god monitorering av vitala funktioner som andning, puls och blodtryck. Postop har i regel ett stort antal patienter samtidigt och det är viktigt att alla är väl monitorerade och att eventuella komplikationer upptäcks i tid och åtgärdas snabbt. Exempel på allvarliga komplikationer kan t ex vara apnéer eller andningssvikt, blödning eller uttalat blodtrycksfall. Rekommenderade tider för postoperativ övervakning finns på annan plats i narkosguiden.
I uppvakningsfasen är det viktigt att patienten vaknar på ett betryggande sätt med adekvat smärtlindring. Denna ges antingen intravenöst eller i form av blockader med lokalanestesimedel. Många patienter kommer med en epiduralanestesi (EDA) som antingen har startats eller ska startas på postop. Eventuell antibiotikaprofylax ska ges liksom trombosprofylax vid rätt tidpunkt. Eventuella sårdrän och ventrikeldrän ska kontrolleras att de fungerar och okontrollerad blödning måste upptäckas i tid. Eventuella röntgenundersökningar kan behöva genomföras. Justeringar av blodtryckshöjande och inotropa medel som infusion av noradrenalin görs kontinuerligt. Mätning av timdiures görs i relevanta fall. Illamående kan behöva förebyggas och behandlas med antiemetika (PONV). Blodgaser och laboratorieparametrar kan behöva kontrolleras och följas.
Patienter som genomgått större ingrepp eller är instabila efter operation väcks många gånger inne på den postoperativa avdelningen. Extubationen här liknar den på operation men patienten är i regel inte längre påverkad av inhalationsmedel. Kroppstemperaturen bör ligga över 36 grader och arteriella blodgaser följs ofta. Efter genomgången uppvakningsfas kan patienten flyttas över till en kirurgisk vårdavdelning för fortsatt vård och behandling eller om det handlar om dagkirurgiska ingrepp skrivas ut till hemmet. Före hemgång gäller särskilda rutiner för att detta ska fungera på ett betryggande och säkert sätt.
Pocketguide – Anestesi

Pocketguide med kondenserad information om inhalationsmedel, muskelrelaxantia, inhalationsanestesi, vasopressorer, opioider, antiemetika, reversering och malign hypertermi.
Standardanestesi

Induktion för hand med Propofol och Fentanyl. Underhåll med Fentanyl i v och Sevofluran i inhalation. Muskelrelaxantia v b.
Muskelrelaxantia
Muskelrelaxerande läkemedel ger en neuromuskulär blockad genom aktivitet i den neuromuskulära kopplingen i tvärstrimmig muskulatur som styr kraften i muskler och andning. Muskelrelaxantia används för att underlätta för kirurgi i samband med allmän kirurgi särskilt laparoskopisk kirurgi, bukkirurgi, ortopedisk kirurgi, neurokirurgi, thoraxkirurgi eller annan kirurgi där det är nödvändigt att patienten ligger helt still eller är muskelslapp. Neuromuskulär blockad används även för att få kontroll över luftvägen med bra intubationsförhållanden och för att bättre kunna ventilera lungsjuka patienter.

Dosering av muskelrelaxantia
| Preparat | Läkemedelsnamn | Intubationsdos mg/kg | Upprepningsdos = ED95 (mg/kg) |
|---|---|---|---|
| Succinylkolin | Celocurin | 1-1,5 | |
| Mivakurium | Mivacron | 0,2-0,25 | 0,04-0,08 |
| Atrakurium | Atracurium | 0,5-0,6 | 0,2-0,3 |
| Vekuronium | Norcuron | 0,08-0,1 | 0,03 |
| Rokuronium | Esmeron | 0,6-0,9 | 0,2-0,3 |
| Cisatracurium | Nimbex | 0,15-0,2 | 0,06-0,08 |
| Pankuronium | Pavulon | 0,08-0,1 | 0,03 |
Axon från nervändar kopplas normalt till muskelfibrer via ”neuromuskulära junctions” i motorändplattan där neurotransmittorsubstanser släpps ut från presynaptiska vesikler och förmedlar den neuromuskulära innervationen. Från dessa synapser frisätts acetylkolin som rusar över synapsen och binder till postsynaptiska acetylkolinreceptorer för aktivitet. Acetylkolinreceptorerna är kolinerga receptorer men de kan även aktiveras av nikotin och kallas därför för nikotinreceptorer – nAchR (nikotinerg acetylkolinreceptor). Nikotinreceptorer är en form av ligandstyrda jonkanaler som öppnar en jonkanal när de aktiveras. Detta påverkar vilopotentialen så att nästa nervcell blir benägen att depolarisera och generera muskelkontraktioner.
Muskelrelaxantia är vanligen kvartära ammoniumföreningar som strukturellt liknar acetykolin. Dessa binder till nikotinreceptorns alfa-subenhet och blockerar dessa.
Effektduration av muskelrelaxantia
| Preparat | Läkemedelsnamn | Tid till intubation (min) | Klinisk effekt (min) |
|---|---|---|---|
| Succinylkolin | Celocurin | < 1 | 5-10 |
| Mivakurium | Mivacron | 3-4 | 15-30 |
| Atrakurium | Atracurium | 2-3 | 30-60 |
| Vekuronium | Norcuron | 2-3 | 30-60 |
| Rokuronium | Esmeron | 1-2 | 30-60 |
| Cisatracurium | Nimbex | 3-4 | 45-75 |
| Pankuronium | Pavulon | 2-3 | 45-180 |
Det finns två typer av muskelrelaxantia, depolariserande och icke-depolariserande. Depolariserande muskelrelaxantia (succinylkolin) ger en initial stimulering vilket orsakar en depolarisering med muskelfascikulationer, man kan säga att musklerna aktiveras och laddas ur. Därefter är receptorn stängd för fortsatt nervtransmission tills det muskelrelaxerande ämnet brutits ned av enzymet pseudokolinesteras. Icke-depolariserande muskelrelaxantia binder till den nikotinerga receptorn och blockerar nervtransmissionen, muskelaktiviteten blockeras vanligen under minst 30 min efter induktion.
Succinylkolin ser kemiskt strukturellt ut som en dubbel acetylkolinmolekyl. Vid administrering syns initiala fascikulationer, oftast först synliga runt ögonen omedelbart följt av ansiktet och övriga kroppen. Succinylkolin är snabbverkande med kort duration, effekt sitter vanligen i 5-10 min. Succinylkolin är det muskelrelaxantia som ger bäst intubationsförhållanden och bäst luftvägskontroll. Det används inte bara för att kunna intubera utan även för att lösa laryngospasm och svår bröstkorgsrigiditet, t ex efter överdosering av remifentanil. Den korta durationen beror på redistribution från neuromuskulära junctions, substansen bryts ner av pseudokolinesteras vilket är detsamma som butylkolinesteras och plasmakolinesteras. Det finns en familjär brist av pseudokolinesteras vilket kan göra att vissa patienter får en långvarig muskelrelaxation av succinylkolin. Vanligen släpper dock effekten även hos dessa patienter efter ett par timmar, tillståndet är ovanligt. I dessa fall bör administrering av succinylkolin naturligtvis undvikas. Förlängd effekt av succinylkolin kan uppkomma vid leversjukdom, cancer och nedsatt allmäntillstånd och användning av andra läkemedel som metaboliseras av kolinesteras.
Succinylkolin har vissa biverkningar som frisättning av kalium (cave brännskador), arytmier, bradykardier (små barn), postoperativ muskelsmärta, malign hypertermi och histaminfrisättning. Det bör inte ges till patienter efter långvarig immobilisering (långliggare på IVA!), muskelsjukdomar, brännskador (efter 24 timmar), ryggmärgsskador, plasmakolinesterasbrist, malign hypertermi, intrakraniell tryckstegring eller uremi. Man får dock i varje enskilt fall väga riskerna mot fördelarna. Etableringen av fri luftväg har alltid högsta prioritet hos medvetslösa eller vakenhetssänkta patienter och där är succinylkolin snabbast och mest effektivt för god luftvägskontroll.
Icke depolariserande muskelrelaxantia är kemiskt strukturellt antingen steroidbaserade eller bensylisoquinolinbaserade estrar. Steroidbaserade icke depolariserande muskelrelaxantia är t.ex. vecuronium och rocuronium som är relativt lika. De steroidbaserade medlen har låg frekvens allergiska reaktioner, passerar inte placenta och metaboliseras genom hydroxylering i levern. Rocuronium är ett medellångverkande medel med aktiva metaboliter vilket innebär viss risk för förlängd effekt vid leversvikt. Det metaboliseras i levern och utsöndras via gallan. Rocuronium är ett alternativ till succinylkolin vid rapid sequens induction (RSI) i högre dosering än normalt, 0,9-1,0 mg/kg. Vid behov kan effekten reverseras med en specifik antidot sugamadex (Bridion).
Pancuronium är ett äldre långverkande medel med relativt hög muskarinerg aktivitet som sällan används idag. Pancuronium var standardmedel för anestesiologisk muskelrelaxation fram till 90-talet.
Det finns ett flertal andra icke depolariserande medel som farmakologiskt kategoriseras som bensylisoquinoliner. Medlen har relativt låg muskarinerg affinitet. Bland dessa medel märks atrakurium, cisatrakurium och mivakurium. Dessa medel har relativt hög histaminfrisättande effekt som kliniskt riskerar att ge hudrodnad och bronkkonstriktion. Atrakurium och cisatrakurium bryts ner av ospecifika plasmaesteraser och har en spontan kemisk nedbrytning via den s.k. Hoffman elimineringen. Mivacurium bryts ner av pseudokolinesteras. Eliminationen är oberoende av lever och njurfunktion.
Atrakurium är ett medellångverkande icke depolariserande medel med en heterogen sammansättning av isomerer. Atracurium är histaminfrisättande och elimineras via Hoffmaneliminationen.
Mivacuriumär ett kortverkande icke depolariserande muskelrelaxantia. Ger viss histaminfrisättning och bryts ner av pseudokolinesteras.
Reversering
Innan extubation bör neuromuskulär funktion uppmätas via n.ulnaris stimulation. TOF ≥90% accepterats för säker extubation. Rokuronium effekt kan reverseras med Neostigmin eller Sugammadex. Patienten kan extuberas efter att ha bekräftat reverseringen med ett TOF värde ≥90%. Vid TOF <20% rekommenderas Sugammadex. Dosen beror på blockadens djup.
Effekten av icke depolariserande muskelrelaxantia reverseras vanligen med neostigmin som är en kolinesterashämmare varvid muskulär innervation återställs. Neostigmin kan ge bradykardi och bronkonstriktion varför man samtidigt vanligen ger atropin som antikolinergikum. En vanlig reverseringsdos till vuxen är 2,5 mg neostigmin (1 ml) och 0,5 mg atropin (1 ml), sammanlagt 2 ml. Neostigmin kan öka mängden acetylkolin i synapsen och kan konkurrera bort icke-depolariserande muskelrelaxantia. Vid ofullständig reversering kan en halv reverseringsdos ytterligare ges (1/2 ml neostigmin + 1/2 ml atropin). Doseringen av neostigmin är 30-70 mikrog/kg men doseringen standardiseras vanligen till 1 ml (2,5 mg) till vuxen och efter vikten till barn. Effekten av muskelrelaxantia och reversering bör monitoreras kontinuerligt med specifika övervakningssystem.
Malign hypertermi
Råd för behandling av en akut reaktion som vid malign hypertermi
Malign hypertermi (MH) känslighet är ett ärftligt tillstånd där potenta inhalationsanestetika och/eller suxametonium kan utlösa en livshotande reaktion under narkos. Vid en MH-reaktion ses tecken till hypermetabolism och muskelpåverkan. MH-reaktioner är ovanliga och viktiga att identifiera, då de är potentiellt livshotande och botbara. En tidigare komplikationsfri anestesi med MH utlösande medel utesluter inte MH-känslighet.
Utlösande: Celocurin + inhalationsgaser.
Symptom: Muskelrigiditet, tempstegring 1°C/5 min, EtCO2↑, svettning, takykardi
Behandling: Hyperventilera minutventilation x 2-3 med 100% O2, byt till TIVA, koppla bort förgasare, avsluta operationen.
Dantrium startdos: 2,5 mg/kg (i grov pvk/CVK) – upprepa 1 mg/kg tills temperaturen faller.
Medel som kan utlösa en MH-reaktion
- Potenta inhalationsanestesimedel
- Sevofluran (Sevorane®)
- Desfluran (Suprane®)
- Äldre inhalationsanestesimedel – Isofluran, Halotan, Enfluran, Eter etc.
- Depolariserande muskelrelaxantia
- Suxameton (Celokurin® – succinylkolin)
Tecken på en MH-reaktion
De kliniska tecknen på en MH-reaktion kan variera mycket, från få till många. Förloppet kan vara allt från explosivt till mer ”smygande”. Den kliniska diagnosen kan därför vara svår att ställa. En MH-reaktion utvecklas nästan alltid under narkos eller i sällsynta fall omedelbart postoperativt. Inget symptom är patognomont för en MH reaktion. Diagnosen MH reaktion är en uteslutningsdiagnos.
Tidiga tecken från olika organsystem
Metabolism
Ökad metabolism – hypermetabolism (”metabol storm”)
- Tecken på ökad CO2 produktion (EtCO2, el pCO2), takypné. Värdet på CO2 måste ställas i relation till minutvolymen. Om kapnografi saknas så, så inger en hög andningsfrekvens och snabbt förbrukad samt het CO2 absorber misstanke om ökad CO2 produktion.
- Ökad O2 -konsumtion
- Metabolisk och respiratorisk acidos
- Profus svettning
- Marmorerad hud
Muskulatur
- Masseterspasm efter tillförsel av suxameton (Celokurin®). Masseterspasm = ”jaws of steel” som kvarstår i två minuter eller mer.
- Generaliserad muskelrigiditet. Generaliserad muskelrigiditet kommer oftast lite senare i förloppet.
Kardiovaskulärt
- Svårförklarlig takykardi
- Arytmier (ffa. ektopiska ventrikulära slag, VES i bigemini)
- Instabilt blodtryck
Sena tecken
- Snabb temperaturstegring (core temperature). Mät temperaturen centralt; rektalt, blåsa, esofagus eller i CVK. Temperaturstegringen är sekundär till hypermetabolismen dvs. höjd temperatur är inte ett första tecken.
- Hyperkalemi. Momentan hyperkalemi efter tillförsel av suxameton inger även misstanke om muskeldystrofi, t.ex Duchennes muskeldystrofi
- Kraftig stegring av CK (kreatinkinas)
- Kraftig stegring av myoglobin (plasma/urin)
- Mörkfärgad urin (Coca-Cola/portvinsfärgad) (tecken på myoglobinuri)
- Njursvikt
- Allvarliga arytmier eller hjärtstillestånd
- Disseminerad intravaskulär koagulation
- Multipel organsvikt
- Hjärndöd/död
Differentialdiagnoser
- För ytlig anestesi
- Infektion/sepsis
- Otillräcklig ventilation alternativt otillräckligt färskgasflöde
- Fel på narkosapparaten
- Iatrogen temperaturstegring
- Annan neuromuskulär sjukdom
- Anafylaktisk reaktion, feokromocytom, tyreotoxisk kris, reaktion utlöst av ecstasy eller annan centralstimulerande drog, malignt neuroleptikasyndrom (NMS – Neuroleptic Malignant Syndrome).
Behandling
Behandling skall påbörjas omedelbart. Dantrolen har högsta prioritet. Fördröjning av tillförsel av dantrolen ökar mortalitet och morbiditet. Symptomen kan variera avsevärt och behandlingen anpassas därefter.
Omedelbart
- Stoppa tillförseln av alla triggande medel. Lyft av förgasaren. Om det inte går stäng av den.
- Öka till 100% syrgas och öka färskgasflöden till > 10 liter/min.
- Hyperventilera 2 – 3 gånger normal minutvolym med 100% syrgas.
- Informera alla på salen och kalla på hjälp. Begär att få in dantrolen. Det krävs gott om personal för att blanda dantrolen, ta prover, ordna infarter etcetera.
- Byt till total intravenös anestesi. Ödsla inte tid här på att byta slangar eller narkosapparat, det kan göras senare. Dantrolen har högsta prioritet.
- Fatta beslut om det operativa ingreppet skall/kan avslutas eller inte.
- Om operatören är oerfaren kalla på en erfaren kollega.
Dantrolen (Dantrium®)
- Ge dantrolen 2 mg/kg intravenöst. Ampuller à 20 mg blandas med 60 ml sterilt vatten. Lättast går det med rumstempererat sterilt vatten.
- Upprepa tillförseln tills symptomen klingat av.
- Om det ser ut att bli brist på dantrolen så rekvirera mer från annan sjukvårdsinrättning.
- Maxdosen dantrolen är 10 mg/kg, men den dosen kan i sällsynta fall behöva överskridas.
Monitorering
- Fortsätt påbörjad monitorering (SaO2, EtCO2, EKG, Blodtryck).
- Temperaturmätning centralt (rektalt, blåsa, esofagus eller i CVK). Perifer temperaturmätning är otillförlitligt i denna situation.
- Säkerställ att det finns bra välfungerande venösa infarter.
- KAD, artärnål, och CVK kan komma att behövas. Tillförsel av dantrolen har högre prioritet än CVK och artärnål initialt.
- Labprov
- Blodgas
- Elektrolytstatus
- CK
- Myoglobin
- Blodsocker
- Kreatinin
- Leverstatus
- Koagulationsstatus
- Vid indikation på annan provtagning
- Övervaka/vårda patienten på en intensivvårds- eller postoperativ avdelning i minst 24 timmar efter en MH reaktion. Symptomen kan recidivera och kan behöva behandlas.
- Kompartmentsyndrom kan utvecklas. Kontrollera vid behov.
Symptomatisk behandling
Behandla hypertermi
Hög prioritet.
- Ge 2 -3 liter kall NaCl, Ringer-acetat eller liknande.
- Ytkylning: våta lakan eller is i axiller och ljumskar.
- Andra metoder t.ex. apparat för yt- eller intravenös kylning.
- Sluta kyla patienten när central kroppstemperatur gått ner till ~38 -38,5o Temperaturen kommer att gå ner ytterligare efter att kylningen avslutats. Vid för kraftig kylning finns risk för rebound fenomen.
Behandla hyperkalemi
Hög prioritet.
- Vid livshotande hyperkalemi ge kalcium. T.ex. calcium-gluconate 10-20 ml till vuxen.
- Glukos och insulin iv. Vid behov. t.ex. 20 E ”snabbinsulin” i 1000 ml 5% Glukos 100-200 ml per timma. Mer insulin kan behövas. Kontrollera för hypoglykemi.
- Dialys kan behövas.
Behandla acidos
- Hyperventilera till normokapné, om möjligt.
- Ge Tribonat® eller Natriumbikarbonat om pH< 7,2.
Glöm inte att tillförsel av Natriumbikarbonat ger ökad CO2belastning
Behandla arytmier
- Amiodaron (Cordarone®) 300 mg till vuxen (3 mg/kg)
- β-blockerare vid kvarstående takykardi
- Ge inte kalciumantagonister
Upprätthåll god diures > 2 ml/kg/tim med
- Diuretika t.ex. furosemid eller mannitol. Observera att varje flaska dantrolen innehåller 3 g mannitol.
- Vätska t.ex. Ringeracetat eller NaCl.
Patienter som haft en misstänkt MH-reaktion bör genomgå en MH-utredning med IVCT-test och mutationsanalys. IVCT= in vitro contracture test. Detta test innebär att man tar ut en liten muskelbit som man monterar upp i ett organbad och exponerar för halotan respektive koffein samt stimulerar elektriskt. Enbart negativt mutationstest utesluter inte MH-känslighet. Patientens närmaste släktingar bör informeras.
Referenser
- Glahn KP et al. Recognizing and managing a malignant hyperthermia crisis: guidelines from the European Malignant Hyperthermia Group. Br J Anaesth. 2010 Oct;105(4):417-20.
- Rosenberg H, et al. Malignant hyperthermia: a review. Orphanet J Rare Dis. 2015;10:93.
- Hopkins PM,et al. European Malignant Hyperthermia Group guidelines for investigation of malignant hyperthermia susceptibility. Br J Anaesth.2015 Oct;115(4):531-9.
- Hyperkalemi http://www.internetmedicin.se/page.aspx?id=899 ( nedladdat 2017-02-26)
Det finns en app för iPhone som kan vara till hjälp:
Appstore: MHapp – Malignant Hyperthermia








