Författare:
Uppdaterad:
14 december, 2023
Här beskrivs de fysikaliska principerna för dialys och metoder för dialys på en intensivvårdsavdelning. Här finns beskrivet olika metoder som CRRT med CVVHDF, Ultrafiltration, peritonealdialys, plasmaferes och MARS behandling. Här finns också ett inlagt kompendium om dialysbehandling.
- Dialysbehandling
- Citratdialys
- CRRT
- CVVH – Continuous Veno Venous Hemofiltration
- CVVHD – Continuous Veno Venous Hemodialysis
- CVVHDF – Continuous Veno Venous Hemodiafiltration
- CRRT – kompendium
- Kontinuerlig Veno-Venös Dialys (CVVHF)
- Hemodialys (HD)
- Peritonealdialys (PD)
- Plasmaferes
- MARS (Molecular Adsorbent Recirculating System)
Dialysbehandling
Dialysbehandling ges vid akut eller kronisk njursvikt med uremi. Akut njursvikt är en vanlig följd av olika livshotande sjukdomar som t ex sepsis, akut leversvikt, stort trauma, akut pankreatit m m och dialysbehandling är ett vanligt inslag på en intensivvårdsavdelning. Akut njursvikt ökar mortaliteten vid olika allvarliga sjukdomstillstånd och rätt insatt dialysbehandling kan många gånger förbättra prognosen och rädda liv. I detta kapitel beskrivs olika typer av dialysmetoder som används inom intensivvården.
Det finns många sätt att mäta njurfunktionen, vanligen används bestämning av kreatinin, urea och formelberäkning av GFR. För mer noggrann bestämning används oftast iohexolclearance eller krom-EDTA-clearance. För uppskattning av njurfunktionsnedsättningen duger formelclearance (eGFR) ganska bra. Njurfunktionen sjunker påtagligt med åldern medan p-kreatinin stiger mindre.
Referensvärden för GFR
| 20-50 år | 80-125 ml/min/1,73 m2 |
| 51-65 år | 60-110 ml/min/1,73 m2 |
| 66-80 år | 50-90 ml/min/1,73 m2 |
Generella indikationer för dialysbehandling
- Urea > 40 mmol/l
- Terapiresistent hyperkalemi
- Lungödem med FiO2 > 0,8 trots diuretika och PEEP (upp till 10 cm H2O)
- Hypervolemi vid chock, sepsis eller akut leversvikt
- Vissa förgiftningar, t ex metanol-, metformin- eller etylenglykolförgiftning
Olika stadier av njursvikt (CDK - chronic kidney disease)
| CKD 1 | GFR > 90 ml/min | Normal njurfunktion |
| CKD 2 | GFR 60-90 ml/min | Nedsatt njurfunktionsreserv Inga symtom |
| CKD 3 | GFR 30-60 ml/min | Asymtomatisk njursvikt Fosfatretention Nedsatt syntes av 1,25 VitD3 Nedsatt syntes av erytropoietin |
| CKD 4 | GFR 15-30 | Symtomatisk njursvikt Kliniska symtom, elektrolytstörningar, kalcium fosfatrubbningar, anemi, metabolsik acidos, uremiska symtom |
| CKD 5 | Avancerad terminal njursvikt | Uttalade uremiska symtom Vätskeretention |
Det finns flera typer av dialys som används på särskilda dialysavdelningar eller på en intensivvårdsavdelning. De vanligaste formerna är hemodialys (HD), kontinuerlig veno-venös dialys (CVVHF), plasmaferes, peritonealdialys (PD) eller MARS-behandling (molecular reabsorbent recirculating system). Den vanligaste formen av dialys på en intensivvårdsavdelning idag är venovenös kontinuerlig dialys som görs genom en och samma dialyskateter, vanligen en variant av CVK med två eller tre lumen som benämns central dialyskateter (CDK). Peritonealdialys ges sällan eller aldrig på en intensivvårdsavdelning och MARS-behandling ges vid enstaka tillfällen på regionala centra för behandling av akut fulminant leversvikt, oftast som en brygga inför levertransplantation.


Dialys fungerar genom perfusion av blodet genom ett filter varvid blodet renas genom osmos och filtrering av molekyler som urea och kalium. I dialys används två huvudsakliga principer för rening av blodet, diffusion och konvektion. Med diffusion utnyttjas koncentrationsgradienten över ett semipermeabelt membran så att molekyler transporteras över filtret, ungefär som te som diffunderar ut ur en tepåse i hett vatten. Diffusion är effektivt för att eliminera små molekyler utan volymsförlust. Clearance uttrycker utsöndrad mängd av en substans via njurarna som beror på urinkoncentrationen och urinvolymen. Renalt clearance uttrycker sambandet mellan utsöndringen av en substans per tidsenhet och dess koncentration i plasma, Cx = Ux x V/Px ml/min. Med clearance kan man jämföra njurens eller dialysmaskinens förmåga att utsöndra olika substanser. Clearance beror på blodflödet genom filtret och mängden dialysvätska per minut. Diffusionsprincipen används vid hemodialys, CVVHD och CVVHDF.
Konvektion renar blodet genom en tryckgradient som gör att molekyler pressas genom ett membran tillsammans med vätska ungefär som när man brygger kaffe. Med konvektion kan även större molekyler filtreras beroende på membranets storlek och porernas storlek, jämför med ett stort eller litet kaffefilter. Eftersom antalet porer för stora molekyler är färre än för mindre molekyler mättas filterförmågan snabbare för större partiklar än för små. Med konvektion får man även en vätskeförlust som man kan ersätta i dialysen med ersättningslösningar varigenom vätskebalansen kan styras. Clearance varierar med volymen av vätskeborttaget per tidsenhet och volymen på ersättningsvätskan. Principen med konvektion används vid dialysformerna SCUF, CVVH och CVVHDF.
De generella indikationerna för behandling med dialys är uremi med urea > 40 mmol/l (relativ indikation vid urea 30-40 mmol/l), terapiresistent hyperkalemi, lungödem med FiO2 > 0,8 och samtidig övervätskning och diuretikaresistens. Vid akut livshotande lungödem med kronisk eller akut njursvikt är SCUF den metod som snabbast kan förbättra tillståndet liksom behandling med PEEP i ventilator eller CPAP.
Vanligen styrs behandling med CVVH, CVVHD och CVVHDF av intensivist eller anestesiolog medan behandling med plasmaferes, MARS, hemodialys eller PD styrs av en njurmedicinare. Det är därför nödvändigt för en anestesiolog att vara väl förtrogen med den kontinuerliga dialysformen som ges via CDK.
Vid uppstart av CRRT med kontinuerlig dialys på IVA ordineras vanligen grundinställningar i dialysmaskinen. Dessa inställningar varierar med typ av dialysmaskin men vanligen ordineras först en avflödesdos och en vätskefördelning. Avflödesdosen startar vanligen på 30 ml/kg/tim vilket är detsamma som effluentdosen. Avflödesdosen är summan av dialysat, ersättningsvätska pre- och post filter samt vätskeborttag. Vid sepsis, grav leversvikt, brännskada eller annat katabolt tillstånd kan man överväga att starta högre med ett totalt avflöde om 35-40-60 ml/kg/tim.
Förslag på inställningar i CVVHDF vid start
| Standard | Sepsis | |
|---|---|---|
| Blodflöde | 250 (≥150) mL/min | 250 ml/min eller mer |
| Avflödesdos | 30 ml/kg/h | 35 ml/kg/h eller mer |
| Dialysat (ml/h) | 2⁄3 av avflödesdos | 1⁄3 av avflödesdos |
| Ersättning | 1⁄3 av avflödesdos (alltid ≥ 0,5 l post filter) | 2⁄3 av avflödesdos (alltid ≥ 0,5 l post filter) |
| Bolus | 0-10 IE/kg | 0-10-20 IE/kg |
| Kontinuerlig infusion | 0-10-20 IE/kg/h (ofta 1-2 ml/h med Heparin 500 enh/ml) | 0-10-20 IE/h (ofta 1-2 ml/h med Heparin 500 enh/ml) |

Fördelningen mellan ersättningsvätska och dialysvätska beror på vilken storlek partiklarna har som man vill eliminera i första hand. Elimination av stora partiklar kräver mer ersättningsvätska medan mindre molekyler kräver mer dialysatvätska. Inställningarna beror också på vilken dialysmaskin som används. Prismaflex kräver minst 500 ml post filter. Med ökad mängd vätska efter filtret får man en effektivare dialys men större risk för filterstopp. Predilution minskar risken för filterstopp men ger en större spädningseffekt av blodet som skall dialyseras. Effekten av dialysen kontrolleras genom daglig mätning av urea och kreatinin samt vägning av patienten och beräkning av vätskebalansen.
Blodflödet i dialysmaskinen vid CRRT varierar vanligen mellan 100 och 250 ml/min, numera är det vanligare att man ligger mellan 200-250 ml/min. Fördelen med ett högt blodflöde är att mängden dilayserat blod ökar per tidsenhet vilket gör dialysen effektivare, att man motverkar att blodet uppnår samma koncentration som dialysatet i slutet av filtret. Med ökat blodflöde motverkas denna benägenhet och effekten av dialysen ökar. Med ett högt blodflöde minskar också risken för stopp i filtret. Med SCUF, CVVH och CVVHDF utan predilution riskerar man att få en hemokoncentration med högt EVF som kan reducera filtrets livslängd. Filtrationsfraktionen (FF) definieras som den mängd vätska som tas bort i förhållande till mängden blod som passerar filtret.
Vid dialysbehandling ges samtidigt antikoagulation om patienten inte redan är påtagligt lättblödande för att öka dialysfiltrets livslängd. Vanligen används heparin. Antikoagulation ges för att inte blodet skall koagulera vid kontakt med plastslangar och dialysfilter. Koagulationsaktiveringen minskas också av att man späder blodet genom predilution. Vanligen ges heparin i låg koncentration först som en bolusdos, därefter i kontinuerlig infusion. I bolus ges vanligen 10 IE/kg följt av 10 IE/kg/tim. Om dialysfiltret koagulerar redan inom 24 h, kan dosen heparin höjas till 15 IE/kg i bolus följt av 15 IE/kg/tim. Effekten kontrolleras mot PK-INR och APTT. Dialysens effektivitet begränsas av dialysfiltrets livslängd. När filtrets livslängd är begränsad kan inställningarna i dialysen korrigeras eller så kan antikoagulationen korrigeras. Vid många tillfällen kan patientens dialyskateter behöva bytas eller lägeskorrigeras för att få en fungerande kontinuerlig dialys.
Om filtertid är mindre än 24 h
- Räkna ”Filtration Fraction” (dragning vs flöde)
- Om FF < 20-30%: Öka predilutionen eller blodflödet
Justera antikoagulationen (heparininfusion)
- Ge Heparin 15 IE/kg bolus + öka infusionen med 5 IE/kg
- Mät APTT (som bör ligga i övre normalintervallet)
Citratdialys
Som alternativ till heparin i dialysmaskinen kan man ge citrat i infusion som antikoagulation. Metoden kallas för regional citratantikoagulation (RCA). Citrat infunderas i dialysmaskinens blodkrets vilket binder calcium varvid blodet blir mer lättflytande och koagulerar inte i filtret. Calcium bildar ett komplex med citrat som huvudsakligen utsöndras i ultrafiltratet. Man kan säga att citrat konsumerar calcium och detta måste man kompensera för vid citratdialys genom kontinuerlig intravenös calciumsubstitution. Ett visst överskott av citrat kan gå över i patientens blod och metaboliseras då till bikarbonat. För att patienten inte ska få hypokalcemi ges en kontinuerlig infusion av kalcium i blodbanan som substitution, vanligen via samma kateter som dialysen ges genom. För detta ändamål används vanligen en trelumen CDK. Kalcium kan alternativt ges som substitution i en annan CVK.

Citratdialys går bra att använda även vid allmänpåverkan och vid koagulationsstörningar, även trombocytopeni. Citratdialys lämpar sig däremot inte för patienter med uttalad leversvikt eller chockbild med nedsatt mikrocirkulation. Citratdialys tolererar betydligt lägre blodflöde i dialysmaskinens blodkrets jämfört med heparininfusion, vanlig inställning i blodflöde är 100-150 ml/min mot 200-250 ml/min för heparinbaserad dialys. Antikoagulationen med citrat är vanligen väldigt effektiv och ger längre filtertider jämfört med heparinbaserad antikoagulation.
Vid citratdialys föreligger en liten risk för citratackumulation med risk för hypocalcemi. Detta regleras genom justering av citratdosen och calciumsubstitutionen. Vanligen startar man behandlingen med en citratdos om 3,0 mmol/l i dialyskretsen och en calciumkompensation om 100 % som ges till patientens blod i CDK:n. Calciumkompensationen ges med Kalciumklorid APL, 500 µmol/ml (20 mg/ml). Calcium mäts regelbundet i dialyskretsen (Postfilter-Ca = Pf-Ca2+) och i patientens blod (S-Ca2+) varvid man får en Pf-Ca/S-Ca2+-kvot som kan indikera citratackumulation. På patienter som visar tecken till citratackumulering efter ett dygns behandling (ökat behov av intravenös calciumsubstitution, Pf-Ca/S-Ca2+-kvot > 2,4,) minskas i första hand citratdosen i steg om 0,5 mmol/l.
Ordination vid CRRT och RCA
- Dialyskateter
Trippellumen dialyskateter används vid CRRT med RCA. Tredje lumen används för calciuminfusion. - Modalitet
Utgå från CVVHDF. - Priming
I normalfallet primas CRRT med heparin. Vid misstänkt eller konstaterad Heparininducerad trombocytopeni (HIT) sker priming utan heparin. - Citratkoncentration
Initialt väljs citratkoncentration 3 mmol/L (”Citratdos” på PrisMAX). Dialysmaskinen upprätthåller en konstant citratkoncentration i den extrakorporeala kretsen genom att justera pumpen som tillför den citratinnehållande lösningen (PBP-pump). - Calciumkompensation
Initialt väljs 100%. Det innebär att 100% av calciumförlusterna i avflödet ersätts. Infusion av CaCl titreras till joniserad Ca2+ i blodet 1.0–1.3 mmol/L. Kompensationen kan justeras mellan 25–200%. Dialysmaskinen beräknar flödeshastigheten och justerar automatiskt när andra flödeshastigheter förändras för att bibehålla graden av kompensation. - Blodflöde och dialyslösningar
Utgå initialt från tabell 1 (se nedan) och ordinera blod-, dialysat- och ersättningsflöde post filter efter patientens BMI-justerad idealvikt. Dialysmaskinen kommer efter ordinerat blodflöde ställa in ersättningsflödet pre filter (PBP-pump) med citratlösningen automatiskt för att uppnå ordinerad citratkoncentration. När blodflödet ändras kommer hastigheten på PBP-pumpen samt calciumtillförsel justeras automatiskt för att uppnå inställd citratkoncentration och calciumkompensation.
Citratdialys (normala inställningar)
| Vikt (kg) | Blodflöde (ml/min) | Dialysatflöde (ml/tim) | Ersättningsvätska post-filter (ml/tim) | Avflödesdos (ml/kg/h) |
|---|---|---|---|---|
| 50 | 110 | 1000 | 200 | 37 |
| 60 | 110 | 1100 | 400 | 37 |
| 70 | 120 | 1200 | 500 | 35 |
| 80 | 130 | 1300 | 500 | 33 |
| 90 | 140 | 1400 | 500 | 31 |
| 100 | 150 | 1500 | 600 | 31 |
| 110 | 160 | 1600 | 700 | 30 |
| 120 | 170 | 1700 | 800 | 30 |
| 130 | 180 | 1800 | 1000 | 30 |
Monitorering under behandling av calciumsubstitutionen
S-Ca2+ och Pf-Ca2+ kontrolleras 1 och 3 timmar efter uppstart, därefter var 8:e timme om värdena ligger stabilt. Pf-Ca2+ mäts för att få optimal antikoagulation och S-Ca2+ för att säkerställa att
calciumsubstitutionen är tillräcklig.
Citratdosering och calciumsubstitution vid regional citrat antikoagulation
Nivåer av calcium postfilter respektive i serum
| Nivåer av calcium postfilter respektive i serum | Pf-Ca2+ >0,50 mmol/l | Pf-Ca2+ 0,25-0,50 mmol/l | Pf-Ca2+ <0,25 mmol/l |
|---|---|---|---|
| S-Ca2+ <1,00 mmol/l | Citratdosen ökas med 0,5 mmol/liter och Calciuminfusionen ökas med 5-15 % | Calciuminfusionen ökas med 5-15 % | Citratdosen minskas med 0,5 mmol/liter |
| S-Ca2+ 1,00-1,2 mmol/l | Citratdosen ökas med 0,5 mmol/liter | Inga ändringar | Citratdosen minskas med 0,5 mmol/liter |
| S-Ca2+ >1,20 mmol/l | Calciuminfusionen minskas med 5-15 % | Calciuminfusionen minskas med 5-15 % | Citratdosen minskas med 0,5 mmol/liter och Calciuminfusionen minskas med 5-15 % |
Om S-Ca2+ är under 0,80 mmol/l, ges samtidigt bolusdos Calciumgluconat (10 mg/ml) 10 ml iv.
Metabol kontroll
Metabola korrigeringar sker i första hand med ändring av dialysatflödet som är förhållandevis buffertfattigt.
Alkalos: Öka dialysatflödet (Biphozyl) med 250 ml/tim per 3 mmol/l önskad BE-ändring. Överväg att sänka citratdosen så Pf-Ca ligger nära 0,5 mmol/l.
Acidos: Minska dialysatflödet 250-500 ml/tim. Överväg extra buffring med natriumbikarbonat iv. Överväg möjligheten till citratackumulering med vägledning av kvoten P-Ca/S-Ca2+>2,4 och i så fall minska citratdosen i steg om 0,5 mmol/l.
Vanliga inställningar vid behandling med CVVHDF
| Vanlig inställning | Möjliga variationer | Behandling vid sepsis | |
|---|---|---|---|
| Blodflöde | 250 ml/min | 10-450 ml/min | 250 ml/min eller mer |
| Avflödesdos | 30 ml/kg/tim | 0-8000 ml/tim | 35 ml/kg/tim eller mer |
| Ersättningsvätska | 10 ml/kg/tim, alltid > 0,5 l efter filtret | 50-8000 ml/tim | 20 ml/kg/tim, alltid > 0,5 l efter filtret |
| Dialysat | 20 ml/kg/tim | 50-4000 ml/tim | 10 ml/kg/tim |
| Vätskeborttag | 100-200 ml/tim | 0-2000 ml/tim | Anpassas efter status |
| Bolus Heparin | 0-10 IE/kg | 0-10 IE/kg | 0-10-20 IE/kg |
| Kontinuerlig infusion Heparin | 0-5-10-20 IE/kg/tim | 0-5-10-20 IE/kg/tim | 0-5-10-20 IE/kg/tim |
Exempel på normala inställningar i dialysmaskin vid kroppsvikt 70 kg i CVVHDF
| Blodflöde | 250 ml/min |
| Avflödesdos | 2100 ml/tim |
| Ersättningsvätska | 700 ml varav 500 ml post filter |
| Dialysat | 1400 ml |
| Vätskeborttag | 125 ml/tim |
| Bolusdos heparin | 700 IE |
| Kontinuerlig infusion heparin | 350-700 IE/tim |
CRRT
Målsättningen med all njurersättningsterapi (CRRT) är att avlägsna ett pga. njursjukdom uppkommet överskott av slaggprodukter och vatten från kroppen. Hur effektivt ett ämne avlägsnas brukar anges som clearance (K) av ämnet i fråga. Nedsatt njurfunktion yttrar sig i en sänkning av glomerulusfiltrationen (GFR). Urinens volym beror till viss del på glomerulusfiltrationen, men också på förmågan att återresorbera vatten. Om GFR är noll så blir också urinvolymen noll, dvs. anuri föreligger. Av en normal GFR på ca 150 ml/min (9 liter/timme) återresorberas 99 % och endast 1 % (ca 90 ml/timme) utsöndras som urin. GFR kan alltså vara kraftigt sänkt utan att urinmängden påverkas, om mer än 1 % av GFR utsöndras som urin.
GFR (bildningen av primärurin) kan inte mätas utan måste istället beräknas utifrån njurens förmåga att utsöndra en modellsubstans, dvs. clearance (K) av modellsubstansen i fråga. För att ge ett korrekt mått på GFR måste en sådan modellsubstans filtreras fritt tillsammans med vatten och får inte återresorberas eller utsöndras via tubuli .
K definieras i detta sammanhang som den volym plasmavatten som fullständigt renas från ett ämne under en viss tid och uttrycks oftast i ml/min. K kan beräknas för vilket ämne som helst men det är bara om det filtreras fritt och inte återresorberas eller utsöndras via tubuli som K motsvarar GFR. Kreatinin är den kroppsegna substans som oftast används för att uppskatta GFR.
Två friska njurar åstadkommer ett GFR på ca 150 ml/min vilket kan jämföras med den kontinuerliga njurersättningsterapin (continuous renal replacement therapy; CRRT) som i bästa fall bara är en tredjedel så effektiv.
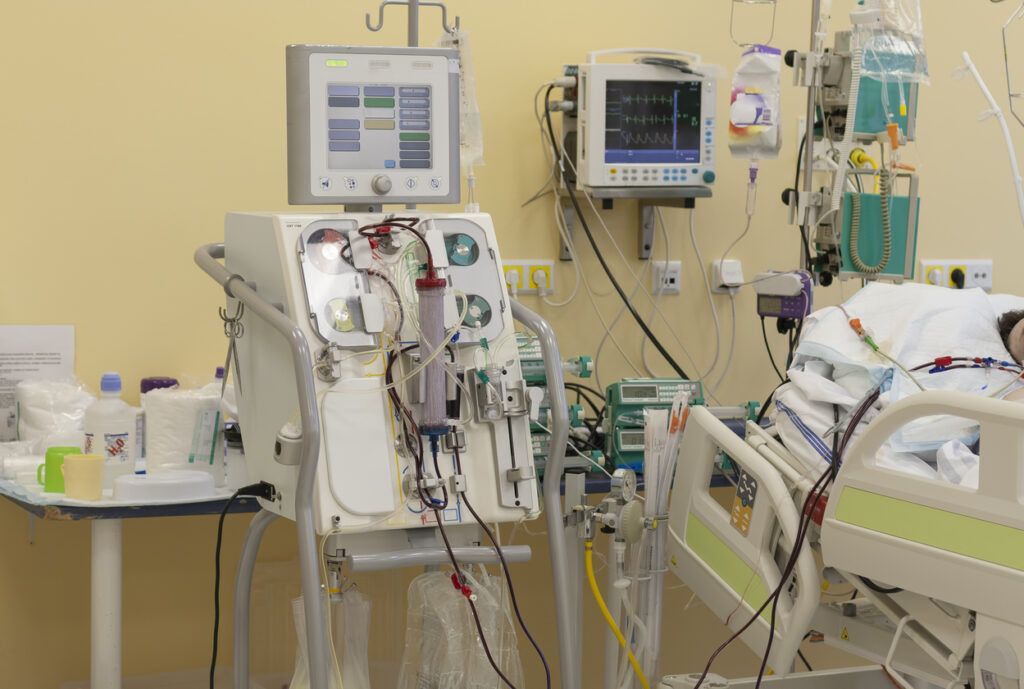
CRRT kan avlägsna vattenlösliga substanser via två olika principer (Figur 1):
- Konvektion (hemofiltration) – då vatten (via ultrafiltration) och däri lösta substanser transporteras över dialysfiltret från blodbanan. Detta åstadkommer CRRT maskinen genom att skapa en tryckgradient (transmembrantryck) över filtret. Clearance (K) bestäms av hur stort ultrafiltrationsflöde över membranet som uppnås.
- Diffusion (hemodialys) – substanser (men inget vatten) diffunderar passivt över dialysfiltret från blodbanan (hög koncentration av substansen) till dialysvätskan (låg koncentration av substansen). Clearance bestäms då av vilken hastighet dialysvätskan har.
Figur 1. CRRT principer för filtration och dialys. PB hydrostatiskt tryck på blodsidan. PUF hydrostatiskt tryck på ultrafiltratsidan. PD hydrostatiskt tryck på dialysatsidan
CRRT kretsen
Moderna CRRT maskiner har förutom blodpumpen även pumpar som driver dialysvätskan, ersättningsvätskan (före och efter filtret) samt ultrafiltratet. Flödet i blodpumpen, i pumpen för ersättningsvätskan före filtret (predilutionspumpen), i pumpen för ersättningsvätskan efter filtret (postdilutionspumpen) samt pumpen för dialysvätskan kan regleras separat inom tämligen vida intervall. Flödet i avflödespumpen (som driver ut ultrafiltratet) kan däremot inte ställas in manuellt utan beräknas av maskinen så att en lagom tryckskillnad (TMP) uppstår över filtermembranet. Flödet i avflödespumpen är summan av flödet i predilutionspumpen, postdilutionspumpen samt det vätskeborttag som önskas varje timme. Samtliga pumpar är integrerade och kopplade till larmfunktioner. Om ett larm utlöses i en pump kommer alla pumpar (utom blodpumpen) att stanna samtidigt. Detta reducerar risken för att problem uppstår i hela kretsen.
Genom att styra de olika pumparna kan den kontinuerliga njurersättningsterapin ges i form av ultrafiltration (CVVH), dialys (CVVHD) eller en kombination av båda (CVVHDF). Nedan följer en beskrivning av CRRT kretsen vid de olika modaliteterna.
SCUF – Slow Continuous Ultrafiltration
Vid den enklaste formen av CRRT består den aktiva flödeskretsen endast av blodpumpen och avflödespumpen (Figur 2). Blodet pumpas från patienten med hjälp av blodpumpen in i filtret. Detta åstadkommer ett positivt hydrostatiskt tryck på filtrets blodsida som överskrider trycket på ultrafiltratsidan något. Denna tryckskillnad över membranet kallas transmembrantryck (TMP). TMP medför att en liten mängd plasmavatten (det s.k. ultrafiltratet) kan ”tryckas” över från blodsidan till ultrafiltratsidan. Genom att använda ytterligare en pump (avflödespumpen) som aktivt ”suger” ut ultrafiltratet från filtret åstadkommer man ett negativt hydrostatiskt tryck på ultrafiltratsidan. Därmed ökar tryckskillnaden (TMP) över membranet markant och den konvektiva ultrafiltrationen ökar. Genom att minska eller öka TMP kan mängden ultrafiltrat regleras exakt.
Det inställda flödet i avflödespumpen motsvarar alltså den volym plasmavatten som avlägsnas från patientens blodbana per tidsenhet. Denna CRRT modalitet brukar kallas SCUF (slow continuous ultrafiltration).
Figur 2. SCUF – Slow Continuous Ultrafiltration
Målsättningen med SCUF behandlingen är endast att avlägsna patientens vattenöverskott. Kom ihåg att i det plasmavatten som transporteras över membranet även finns lösta molekyler, t.ex. kreatinin och urea. Det kreatinin- eller urea-clearance som maskinen åstadkommer vid denna modalitet bestäms alltså helt av flödet i avflödespumpen, dvs. vätskeborttaget.
Om flödet i avflödespumpen är 200 ml/h kommer alltså det konvektiva ultrafiltrationsflödet över membranet att vara 200 ml/h. Clearance (K) för de molekyler som passerar fritt över membranet (t.ex. kreatinin och urea) och som därmed är lösta i ultrafiltratet kommer då att vara: K = Ultrafiltratflödet = 200 ml/h, vilket kan skrivas om som 3,3 ml/min. Med denna inställning kan vi alltså avlägsna vattenöverskottet på ett effektivt sätt. Någon effektiv njurersättningsterapi är det däremot inte frågan om.
- K (SCUF) = Ultrafiltratflödet
Kan vi då inte öka vätskeborttaget för att öka clearance av olika molekyler? Jo, CRRT maskinen klarar detta men patientens cirkulation är begränsande. Ett alltför högt vätskeborttag skulle ju antingen dehydrera patienten eller kräva att stora volymer vätska gavs intravenöst.
Hur kan man då avlägsna en adekvat mängd vatten och samtidigt åstadkomma ett högt clearance? Jo, genom att tillföra en ersättningsvätska före (predilution) eller efter (postdilution) filtret kan vi öka ultrafiltrationsflödet över membranet utan att patienten torkar ut.
CVVH – Continuous Veno Venous Hemofiltration
CVVH med postdilution
Vid CVVH med postdilution ges all ersättningsvätska efter filtret. Postdilutionsflödet drivs av en separat pump (Figur 3).
Figur 3. CVVH med postdilution
Syftet med ersättningsvätskan är alltså att bevara en adekvat vätskebalans samtidigt som en stor volym ultrafiltrat kan avlägsnas från patienten. Om man inte vill att patienten skall dras på vätska skall alltså ultrafiltratflödet (hastigheten i avflödespumpen) och ersättningsflödet (hastigheten i postdilutionspumpen) vara lika. Om man istället önskar en negativ vätskebalans måste alltså ultrafiltratflödet vara större än ersättningsflödet.
- Ultrafiltratflödet = Ersättningsflödet + Vätskeborttaget
Om vi ställer in postdilutionspumpen på t.ex. 3800 ml/h och samtidigt ställer in ett vätskeborttag på 200 ml vätska/h kommer maskinen automatiskt att beräkna hastigheten i avflödespumpen till 3800 ml/h + 200 ml/h = 4000 ml/h. Vad blir då clearance (K) för t.ex. kreatinin och urea i detta exempel?
Kreatinin och urea är små molekyler som passerar fritt över membranet tillsammans med vattnet. K för dessa molekyler blir därför detsamma som ultrafiltratflödet, dvs. 4000 ml/h. Detta kan skrivas som 67 ml/min.
- K (CVVHpostdilution) = Ultrafiltratflödet = Ersättningsflödet + Vätskeborttaget
Den här typen av behandling har dock sina begränsningar. Det höga flödet av plasmavatten över membranet från blodsidan till ultrafiltratsidan kommer att öka blodsidans hematokrit (Hct) påtagligt med risk för att filtret koagulerar. Figur 4 illustrerar hur Hct påverkas på filtrets blodsida vid CVVH med postdilution och ett ultrafiltratflöde på 4 l/h om det inställda blodflödet är 200 ml/min (=12000 ml/h) och patientens Hct=0,3. Hct stiger till 0,45 i slutet av filtret och återgår till 0,31 först efter filtret (där ersättningsvätskan ges).
Figur 4. Hematokrit i filtret vid CVVH med postdilution
Ett sätt att bedöma risken för att filtret skall koagulera vid CVVH med postdilution är att beräkna den s.k. filtrationsfraktionen (FF). FF anger den andel plasmavatten som avlägsnas från blodet vid hemofiltration och kan enkelt beräknas enligt: FF = ultrafiltratflödet/blodflödet. Optimal FF hos en patient med Hct=0,3 är under 20-25 %. Vid en FF över 30 % ökar risken för att filtret skall koagulera markant. Notera att beräkningen av FF inte tar hänsyn till patientens Hct. Det är alltså inte säkert att en hög FF leder till koagulation i filtret om patientens Hct är mycket lågt när blodet når filtret. Omvänt kan en låg FF leda till koagulation i filtret om patientens Hct är högt. Det vanligaste är dock att intensivvårdspatienternas Hct ligger mellan 0,3 och 0,4. I detta intervall ger FF en tillräckligt god uppfattning om risken för koagulering.
- FF = Ultrafiltratflödet/Blodflödet
Ett sätt att komma förbi problemet med hög FF är att ge ersättningsvätskan före filtret (predilution)
CVVH med predilution
Vid CVVH med predilution ges all ersättningsvätska före filtret. Predilutionsflödet drivs av en separat pump (Figur 5).
Figur 5. CVVH med predilution
Blodet som går in i filtret kommer att spädas ut av ersättningsvätskan. Därmed kommer det blod som går in filtret att ha en lägre hematokrit jämfört med patientens äkta hematokrit.
Figur 6 illustrerar hur Hematocrit påverkas på filtrets blodsida vid CVVH med predilution och ett ultrafiltrationsflöde på 4 l/h om det inställda blodflödet är 200 ml/min (=12000 ml/h) och patientens Hct=0,3. Hct stiger visserligen lika mycket i filtret som vid CVVH med postdilution men eftersom Hct är lägre när blodet går in i filtret kommer Hct bara att nå upp till 0,31 i slutet av filtret.
Figur 6. Hematokrit i filtret vid CVVH med predilution
Även CVVH med predilution har sina begränsningar. De slaggprodukter som finns i blodet och som vi vill avlägsna med hjälp av vår njurersättningsterapi kommer att spädas ut av ersättningsvätskan. Ultrafiltratets sammansättning vid CVVH med postdilution består av patientens plasmavatten och däri lösta molekyler. Vid CVVH med predilution består ultrafiltratet av patientens plasmavatten blandad med ersättningsvätska och däri lösta molekyler. Eftersom de lösta molekylerna (t.ex. slaggprodukterna) då har en lägre koncentration så kommer clearance (K) av olika slaggprodukter att vara mindre med denna modalitet jämfört med om ersättningsvätskan ges efter filtret.
För att kunna beräkna clearance vid CVVH med predilution måste man alltså ta hänsyn till hur mycket blodet har spätts ut av ersättningsvätskan. Det görs enklast genom att beräkna den s.k. spädningsfaktorn.
- Spädningsfaktorn = Blodflödet/(Blodflödet + ersättningsflödet före filtret)
I exemplet som illustreras i Figur 6 Hematokrit i filtret vid CVVH med predilution) blir spädningsfaktorn = 12000/(12000 + 3800) = 0,76. Clearance (K) blir då Ultrafiltratflödet x Spädningsfaktorn, dvs. 4000 ml/h x 0,76 ≈ 3000 ml/h.
- K(CVVHpredilution) = Ultrafiltratflödet x Spädningsfaktorn = (Ersättningsflödet+ vätskeborttaget) x Spädningsfaktorn
Jämför Figur 4 och Figur 6. Trots att samma flöden har använts i de båda exemplen så blir clearance 1000 ml/h lägre bara genom att ge all ersättningsvätska före filtret istället för efter filtret.
CVVHD – Continuous Veno Venous Hemodialysis
Vid ren CVVHD avlägsnas molekyler från blodsidan genom diffusion, dvs. molekyler men (i princip) inget vatten passerar över filtret från blodsidan till dialysatsidan. Dialysatvätskan drivs av en separat dialysatpump och det är dialysatvätskans flödeshastighet som avgör clearance (K), dvs hur effektivt blodsidan renas från olika molekyler. Det är förstås möjligt att avlägsna vatten (genom ultrafiltration) även vid denna modalitet men då måste avflödespumpen hålla en högre hastighet än dialysatpumpen. Detta görs genom att det önskade vätskeborttaget ställs in i maskinen (Figur 7).
Figur 7. CVVHD
-
K(CVVHD) = Dialysatflödet
CVVHDF – Continuous Veno Venous Hemodiafiltration
Vid CVVHDF kombineras dialys och filtration (Figur 8). Totalt clearance (K) beräknas enklast genom att först beräkna K för de enskilda modaliteterna och sedan addera dessa.
Figur 8. CVVHDF

Generella indikationer för CRRT
- Urea > 40 mml/l
- Terapiresistent hyperkalemi
- Lungödem med FiO2 > 0,8 trots diuretika och PEEP (upp till 10 cm H2O)
Förslag på inställningar i CVVHDF vid start
| Standard | Sepsis | |
|---|---|---|
| Blodflöde | 250 (≥150) mL/min | 250 ml/min eller mer |
| Avflödesdos | 30 ml/kg/h | 35 ml/kg/h eller mer |
| Dialysat (ml/h) | 2⁄3 av avflödesdos | 1⁄3 av avflödesdos |
| Ersättning | 1⁄3 av avflödesdos (alltid ≥ 0,5 l post filter) | 2⁄3 av avflödesdos (alltid ≥ 0,5 l post filter) |
| Bolus | 0-10 IE/kg | 0-10-20 IE/kg |
| Kontinuerlig infusion | 0-10-20 IE/kg/h (ofta 1-2 ml/h med Heparin 500 enh/ml) | 0-10-20 IE/h (ofta 1-2 ml/h med Heparin 500 enh/ml) |
Om filtertid < 24 h
- Räkna ”Filtration Fraction” (dragning vs flöde)
- Om FF < 20-30%: Öka predilutionen eller blodflödet
Justera v b antikoagulationen (heparininfusion)
- Ge Heparin 15 IE/kg bolus + öka infusionen med 5 IE/kg
- Mät APTT (som bör ligga i övre normalintervallet)
Låt oss illustrera detta med tre exempel. I det första exemplet (1) beräknar vi K vid kombinerad CVVHD och CVVH med postdilution. I andra exemplet (2) beräknar vi K vid kombinerad CVVHD och CVVH med predilution. Slutligen (3) beräknar vi K vid kombinerad CVVHD och CVVH med både pre- och postdilution.
I samtliga exempel förutsätter vi ett blodflöde på 200 ml/min (=12000 ml/h) och ett vätskeborttag på 100 ml/h.
(1) CVVHDF med dialysatflöde = 1000 ml/h och ett postdilutionsflöde = 1000 ml/h.
K(CVVHD) = Dialysatflödet = 1000 ml/h
K(CVVHpostdilution) = Ultrafiltratflödet = Ersättningsflödet + vätskeborttaget = 1000 + 100 = 1100 ml/h
Nu summerar vi helt enkelt bidraget från de olika modaliteterna:
K(CVVHDF) = K(CVVHD) + K(CVVHpostdilution) = 1000 + 1100 = 2100 ml/h vilket är detsamma som 35 ml/min
(2) CVVHDF med dialysatflöde = 1000 ml/h och ett predilutionsflöde = 1000 ml/h.
K(CVVHD) = Dialysatflödet = 1000 ml/h
K(CVVHpredilution) = Ultrafiltratflödet = Ersättningsflödet + vätskeborttaget = 1000 + 100 = 1100 ml/h
Vi summerar bidraget från de olika modaliteterna och får:
K(CVVHDF) = K(CVVHD) + K(CVVHpredilution) + K(vätskeborttaget) = 1000 + 1000 + 100 = 2100 ml/h
I det här exemplet måste vi ta hänsyn till spädningsfaktorn. Eftersom ersättningsvätskan ges före filtret kommer alla substanser som finns i blodet (inklusive de som vi vill avlägsna) att spädas ut. Detta kommer att minska det K som åstadkoms både från dialysen och filtrationen.
Spädningsfaktorn = Blodflödet / (Blodflödet + Ersättningsflödet före filtret) = 12000 / (12000 + 1000) = 0,92
Spädningsfaktorn säger oss att vi, genom att ge ersättningsvätskan före filtret, bara kommer att uppnå 92% av det K som vi annars skulle uppnå om all ersättningsvätska gavs efter filtret.
K(CVVHDF) = 2100 x 0,92 = 1932 ml/h eller 32 ml/min
(3) CVVHDF med dialysatflöde = 1000 ml/h, predilutionsflöde = 1000 ml/h och postdilutionsflöde = 1000 ml/h
K(CVVHD) = Dialysatflödet = 1000 ml/h
K(CVVHpredilution) = Ultrafiltratflödet = Ersättningsflödet före filtret = 1000 ml/h
K(CVVHpostdilution) = Ultrafiltratflödet = Ersättningsflödet efter filtret + vätskeborttaget = 1000 + 100 = 1100 ml/h
Notera att vätskeborttaget bara skall räknas med en gång. Vi har i det här exemplet valt att addera det till ersättningsflödet efter filtret men man hade lika gärna kunnat addera det till ersättningsflödet före filtret – resultatet blir detsamma. Låt oss nu addera bidraget från de olika modaliteterna:
K(CVVHDF) = K(CVVHD) + K(CVVHpredilution) + K(CVVHpostdilution) = 1000 + 1000 + 1100 = 3100 ml/h
Även här måste vi ta hänsyn till spädningsfaktorn. Det är fortfarande bara den ersättningsvätska som ges före filtret (predilutionen) som kan späda ut blodet varför spädningsfaktorn blir densamma som i exempel (2) nämligen 0,92.
K(CVVHDF) = 3100 x 0,92 = 2852 ml/h eller 48 ml/min
- K(CVVHDF) = (K(CVVHD) + K(CVVHpredilution) + K(CVVHpostdilution)) x spädningsfaktorn
Författat av Johan Mårtensson och Claes-Roland Martling, Karolinska Sjukhuset.
CRRT – kompendium
Klicka på bilden för att hämta PDF-filen
 Laddar in …
Laddar in …
Kontinuerlig Veno-Venös Dialys (CVVHF)
Kontinuerlig venovenös hemofiltration kan delas in i alternativt CVVHD alternativt CVVHD-F, kallas ofta för Prismadialys. Prismadialys ger en kontinuerlig ultrafiltration av blodet med eller utan dialys. Metoden drar ut slaggprodukter och vätska från blodbanan. Vattenmolekyler pressas genom ett semipermeabelt membran med hydrostatisk kraft med lägre tryck på dialyssidan.
Indikation: Akut eller kronisk njursvikt med uremi. Övervätskning vid sepsis och annan stor kirurgi. Förgiftning med litium och vissa andra förgiftningar.
Komplikationer: Blodtrycksfall, hypovolemi, muskelkramper, illamående, blödningar, kräkning, huvudvärk, infektion, överkänslighet, hypoxemi, amyloidos.
Teknik: Central dialyskateter (CDK) med dubbellumen läggs vanligen som en CVK i en central ven, normalt i v. jugularis interna dx eller i v. subclavia. Viktigt med röntgenkontroll av kateterläget före användning. Behandlingen ges kontinuerligt dygnet runt i 2-3 veckor. Normalt vätskeborttag är 0,5-2 liter per dygn beroende på patientens vätskebalansstatus. Vanligt blodflöde är 150-250 ml/min och dialysflödet är 500-1500 ml/h. Noggrann viktkontroll, kontroll av uremi och kaliumproblem är viktigt. Ultrafiltration är möjligt med Prismadialys. Drar endast vätska, snabbast effekt vid lungödem.
Rekommenderade inställningar i Prismaflex dialys
| Rekommenderade inställningar i Prismaflex dialys: | ||
|---|---|---|
| Blodflödet ställs normalt in på: | 250-300 ml. | |
| Dialysflöde: | 500-1500 ml/h. | |
| Faktiskt vätskeborttag: | 100-300 ml/h. | |
| Utflödestryck: | -50-75 mm Hg. | |
| Återflödestryck: | 50-100 mm Hg. | |
| Antikoagulation: | Heparin ges i kontinuerlig infusion 500 enh/ml | 0,5-2 ml/h (1 ml/h). |
Rekommenderade flödesinställningar för kontinuerlig venovenös dialys
| Vikt | 50 kg | 60 kg | 70 kg | 80 kg | 90 kg | 100 kg |
|---|---|---|---|---|---|---|
| Pre Blod Pump ml/timme | 375 ml/tim | 550 ml/tim | 725 ml/tim | 900 ml/tim | 1075 ml/tim | 1250 ml/tim |
| Ersättningsvätska ml/timma | 500 ml/tim | 500 ml/tim | 500 ml/tim | 500 ml/tim | 500 ml/tim | 500 ml/tim |
| Dialysvätska flöde ml/timme | 625 ml/tim | 625 ml/tim | 875 ml/tim | 1000 ml/tim | 1125 ml/tim | 1250 ml/tim |
| Blodflöde | 250 ml/timme | 250 ml/timme | 250 ml/timme | 250 ml/timme | 250 ml/timme | 250 ml/timme |
Hemodialys (HD)
Hemodialys ger en rening av blodet genom osmos och dragning av molekyler (urea, kalium) och vätska över ett semipermeabelt membran extracorporealt (utanför kroppen till skillnad från PD).
Indikation
Akut eller kronisk njursvikt med uremi. Övervätskning. Förgiftning med metanol, etylenglykol, litium och vissa andra förgiftningar.
Procedur
Hemodialys görs vanligen genom filtration av blodet genom ett dialysfilter med en yta runt 2 m2 extracorporealt där blodet tas ut ur kroppen, renas och ges tillbaks. Blodet tas ut via grov kärlkateter, fistel eller shunt. Ett vanligt blodflöde (Qb) i dialysfiltret ligger runt 150 ml/min och ett normalt dialysflöde (Qd) runt 500 ml/min. Normalt vätskeborttag är 2-4 liter per dialysbehandling beroende på patientens hemodynamik, uremiska status och aktuellt vätskebalansstatus. Behandlingen genomförs bl.a. via instick i en kirurgisk AV-fistel på över- eller underarmen. En AV-fistel tar 4-8 veckor att mogna. Graft används om tunna, sköra kärl finns hos patienten (ökad risk för trombos och infektion). Central dialyskateter (CDK) med dubbellumen kan användas akut om kärlaccess saknas alternativt via två kärlkatetrar, en artärkateter och en venkateter, vanligen i a femoralis och i v femoralis alt. två venkatetrar. Behandlingen ges intermittent 3-4 dagar i veckan, under 2-4 timmar per behandling. Noggrann viktkontroll och kontroll av urea och kalium är viktigt. Vanligen ges antikoagulation i samband med behandlingen.
Ultrafiltration (UF) är möjligt. Drar endast vätska ur blodbanan, UF ger snabbast effekt vid behandling av lungödem.
Komplikationer till hemodialys är blodtrycksfall, kramper, illamående, kräkning, accessproblem, amyloidos, blödningskomplikationer.
Peritonealdialys (PD)
Peritonealdialys (PD) är en dialysbehandling som utförs normalt via en Tenchoff-kateter genom bukväggen (PD-kateter). PD ger en osmos och dragning av slaggprodukter och vätska över bukhinnan (peritoneum) som sköljs ut med peritonealvätskan. Peritoneum fungerar som dialysfilter. Används ofta initialt vid behandling av kronisk njursvikt. Högst ca 4 års behandlingstid. Bra vid hjärtsvikt (jämnare blodvolym) och för diabetiker (kontinuerlig insulintillförsel). Inflammatorisk tarmsjukdom är en kontraindikation. Kan utföras i hemmet eller på dagvårdsavdelningar. Peritonit och amyloidos (b2-μglobulin) är kända komplikationer. Behandlingen utförs vanligen intermittent 3-4 dagar i veckan, 2-4 timmar per gång. Normalt vätskeborttag är 2-4 liter beroende på om patienten är hemodynamiskt stabil och aktuellt vätskebalansstatus. Noggrann viktkontroll och kontroll av uremi och kaliumproblem är viktigt. Komplikationer till peritonealdialys är främst infektionsproblem, peritonit med eller utan allmänpåverkan.

Plasmaferes
Plasmaferes är en behandlingsform som tar ut venöst helblod och ger tillbaka allt utom plasma. Drar ingen vätska normalt. Ersätter plasman med givarplasma eller albuminlösning, vanligen albuminlösning. Antikroppar, immunkomplex och patologiska proteiner avlägsnas. Används vid TTP/HUS, SLE, Wegeners syndrom, Goodpastures syndrom, Guillain-Barrés syndrom, Myastenia gravis. Central dialyskateter (CDK) med dubbellumen kan användas akut om kärlaccess saknas alternativt en artärkateter, vanligen i a. femoralis och en venkateter i v. femoralis. Behandlingen utförs intermittent 3 dagar i veckan, under 2-4 timmar per gång. Noggrann viktkontroll och kontroll av uremi och kaliumproblem är viktigt.
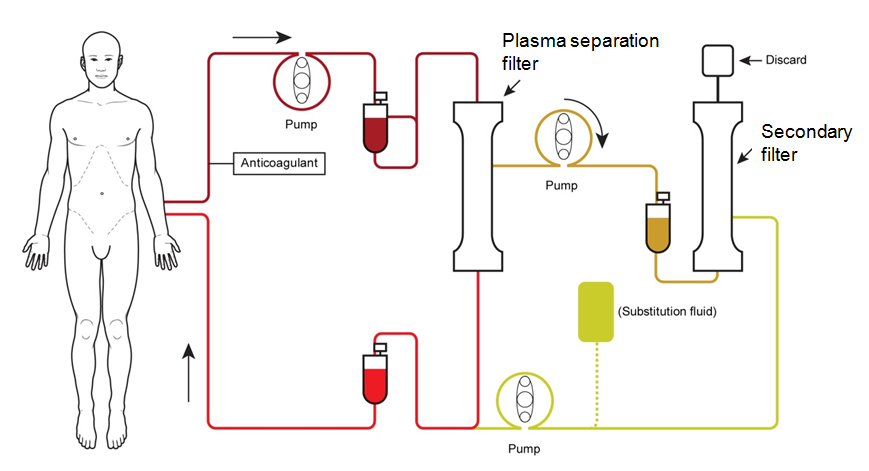
MARS (Molecular Adsorbent Recirculating System)
MARS är en dialysform som tar ut helblod, renar blodet och ger tillbaka allt utom plasma. Drar ingen vätska normalt. Man ersätter plasman med albuminlösning. Man filtrerar blodet genom ett kolfilter och en jonbytare. Antikroppar, immunkomplex och patologiska proteiner avlägsnas. MARS kan användas vid akut leversvikt med encefalopati och vid akut paracetamolförgiftning med leversvikt. Systemet kräver en central dialyskateter (CDK) med dubbellumen som kan användas akut om kärlaccess saknas alternativt en artärkateter, vanligen i a. femoralis och en venkateter i v. femoralis. Behandlingen utförs i 2-3 dagar efter varandra, 4-8 timmar per gång. Noggrann kontroll av uremi och leverfunktion. Risk för blödningskomplikationer. Systemet är resurskrävande, det genomförs vanligtvis på en intensivvårdsavdelning.